
【题目】某化学课外小组用如图装置制取溴本先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
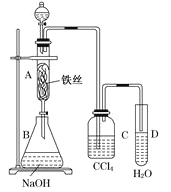
(1)A中铁丝发生如下反应2Fe+3Br2=2FeBr3,FeBr3的作用是_______,请写出A中另外个反应的化学方程式:__________
(2)观察到A中的气体颜色是由_____色变成________色。
(3)实验结束时,打开A下端的活寒,让反应液流入B中,充分振荡,目的是________
(4)C中盛放CCl4的作用是__________
(5)能证明苯和液溴发生的是取代反应,而不是加成反应的方法是验证是否有HBr的生成,故而可向试管D中滴入石蕊溶液,若溶液变红,则能证明。另一种验证的方法是向试管D中加入___________,现象是__________。
【答案】 催化剂 C6H6+Br2![]() C6H5Br+HBr 深红棕 红棕 除去溶于溴苯中的溴,便于观察溴苯的颜色 除去溴化氢气体中的溴蒸气 AgNO3溶液 产生淡黄色沉淀
C6H5Br+HBr 深红棕 红棕 除去溶于溴苯中的溴,便于观察溴苯的颜色 除去溴化氢气体中的溴蒸气 AgNO3溶液 产生淡黄色沉淀
【解析】(1)苯与溴在溴化铁作用下发生取代反应,反应方程式为: C6H6+Br2![]() C6H5Br+HBr,溴化铁作催化剂;正确答案:催化剂;C6H6+Br2
C6H5Br+HBr,溴化铁作催化剂;正确答案:催化剂;C6H6+Br2![]() C6H5Br+HBr。
C6H5Br+HBr。
(2)溴蒸汽颜色为深红棕色,当有部分溴与铁反应生成溴化铁,消耗溴,颜色变浅;正确答案:深红棕;红棕。
(3)溴单质能与氢氧化钠溶液反应而溴苯不能,反应方程式:![]() ═
═![]() ;利用此反应可以除去溴,便于观察溴苯的颜色;正确答案:除去溶于溴苯中的溴,便于观察溴苯的颜色。
;利用此反应可以除去溴,便于观察溴苯的颜色;正确答案:除去溶于溴苯中的溴,便于观察溴苯的颜色。
(4) CCl4能溶解溴不能溶解溴化氢,四氯化碳能除去溴化氢气体中的溴蒸气;正确答案:除去溴化氢气体中的溴蒸气。
(5)如果苯和液溴发生的是取代反应,则有HBr生成;如果发生的是加成反应,则无HBr生成,也就是说,如果要证明苯和液溴发生的是取代反应,而不是加成反应,只需检验有无HBr生成,溴化氢与硝酸银反应生成溴化银淡黄色沉淀;正确答案: AgNO3溶液;产生淡黄色沉淀。


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】水溶液中只可能有K+、Mg2+、AlO2﹣、SiO32﹣、CO32﹣、SO42﹣中的若干种离子.某同学对溶液进行了如图实验:下列判断错误的是( )

A. 有气体甲生成,表明溶液X中一定含有CO32﹣
B. 沉淀甲可能是硅酸镁
C. K+一定存在于溶液X中
D. 不能确定SO42﹣是否存在于溶液X中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据氯水分别与如图四种物质发生的反应选择正确的表述

A. a反应的离子方程式可能是:2Fe2+ +4Br-+3Cl2 =2Fe3+ +2Br2 +6Cl-
B. b反应中产生无色无味气体,说明HClO的酸性强于H2CO3
C. c反应的现象中知可以直接利用硝酸银溶液检验Cl-
D. d反应的最终现象是紫色石蕊溶液褪色,因为Cl2具有漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前“低碳经济”正成为科学家研究的主要课题。请回答下列问题:
Ⅰ.甲烷自热重整是一种先进的制氢方法,其反应方程式为CH4(g)+H2O(g)![]() CO(g)+3H2(g)。
CO(g)+3H2(g)。
(1)阅读下图,计算上述反应的反应热ΔH=________kJ·mol-1。

Ⅱ.用CH4或其他有机物、O2为原料可设计成燃料电池。
(2)以CnH2nOn、O2为原料,H2SO4溶液为电解质设计成燃料电池,则负极的电极反应式为________________________________________________________________________。
(3)以CH4、O2为原料,100mL0.15mol·L-1NaOH溶液为电解质设计成燃料电池,若放电时参与反应的氧气体积为448mL(标准状况),产生的气体全部被溶液吸收,则所得溶液中溶质的成分及物质的量之比为________________________,各离子浓度由大到小的顺序为________________________________________________________________________。
Ⅲ.利用I2O5消除CO污染的反应为5CO(g)+I2O5(s)![]() 5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4molCO,测得CO2的体积分数随时间t变化曲线如下图。请回答:
5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4molCO,测得CO2的体积分数随时间t变化曲线如下图。请回答:
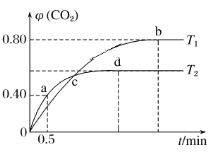
(4)T2时,0~0.5min内的反应速率v(CO)=________________。
(5)T1时化学平衡常数K=________。
(6)下列说法不正确的是________(填标号)。
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的压强相等
C.d点时,增大体系压强,CO的转化率不变
D.b点和d点时化学平衡常数的大小关系:Kb<Kd
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G(分子式为C13H18O2)是一种香料,下图是该香料的一种合成路线。
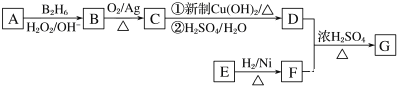
已知:
①E能够发生银镜反应,1molE能够与2molH2完全反应生成F;
②R—CH===CH2![]() R—CH2CH2OH;
R—CH2CH2OH;
③有机物D的摩尔质量为88g·mol-1,其核磁共振氢谱有3组峰;
④有机物F是苯甲醇的同系物,苯环上只有一个无支链的侧链。
回答下列问题:
(1)用系统命名法命名有机物B:________________________________________。
(2)E的结构简式为________________________________。
(3)C与新制Cu(OH)2反应的化学方程式为___________________________。
(4)有机物C可与银氨溶液反应,配制银氨溶液的实验操作为___________________。
(5)已知有机物甲符合下列条件:①为芳香化合物;②与F互为同分异构体;③能被催化氧化成醛。符合上述条件的有机物甲有________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为浓硫酸与铜反应及其产物检验的实验装置
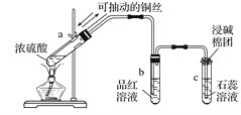
回答下列问题:
(1)指出试管a、b、c中产生的实验现象:
①a中________________________________;
②b中________________________________;
③c中________________________________。
(2)将a试管中的溶液慢慢倒入水中,发生的变化是________________________________。
(3)写出浓硫酸与铜反应的化学方程式:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列有机物的系统命名或结构简式
(1)![]() ________________
________________
(2)![]() ________________
________________
(3)CH3CH(CH3)C(CH3)2(CH2)2CH3________________
(4)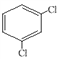 ________________
________________
(5)2,5-二甲基-4-乙基庚烷 ________________
(6)2-甲基-2-戊烯________________
(7)间三甲苯________________
(8)相对分子质量为72且沸点最低的烷烃的结构简式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关阿伏加德罗常数NA的说法正确的是( )
A. 标准状况下,5.6 L CO2与足量Na2O2反应转移的电子数为0.5NA
B. 常温常压下,11gCO2中含有0.75NA个原子
C. 标准状况下,NA个水分子的体积约为22.4L
D. 50 mL 12 mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com