
| A. | Fe3+ | B. | HS- | C. | 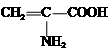 | D. | C6H5O- |
分析 根据离子之间结合生成沉淀、气体、水、弱电解质等,则离子浓度减小,且具有还原性的物质、碳碳双键均能被高锰酸钾氧化,以此来解答.
解答 解:A.Fe3+与盐酸、高锰酸钾均不反应,故A不选;
B.HS-与NaOH固体、少量浓盐酸或少量酸性高锰酸钾溶液均反应,离子浓度下降,故B选;
C.含-COOH与NaOH反应,含氨基与盐酸反应,含碳碳双键与高锰酸钾反应,则都能使该微粒浓度下降,故C选;
D.C6H5O-与NaOH、高锰酸钾均不反应,故D不选;
故选BC.
点评 本题考查离子共存及有机物的结构与性质,为高频考点,把握物质的性质、离子之间的反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 反应物的总键能低于生成物的总键能 | |
| B. | 1mol I2(g)中通入1mol H2(g),反应放热11kJ | |
| C. | 等物质的量时,I2(g)具有的能量低于I2(l) | |
| D. | 平衡时分离出HI(g),正反应速率先减小后增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验编号 | HA | NaOH | 混合溶液的pH |
| 甲组 | c(HA)=0.2mol/L | c(NaOH)=0.2mol/L | pH=a |
| 乙组 | c(HA)=0.1mol/L | c(NaOH)=0.1mol/L | pH=9 |
| 丙组 | pH=2 | pH=12 | pH=b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 萃取 | B. | 渗析 | C. | 蒸馏 | D. | 干馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(K+)=c(HC2O4-)+c(H2C2O4)+2c(C2O42-) | B. | c(Na+)=c(H2C2O4)+c(C2O42-) | ||
| C. | c(K+)+c(Na+)=c(HC2O4-)+c(C2O42-) | D. | c(K+)>c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
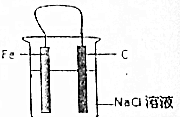 有关Fe-C-Nac1溶液构成的原电池中,叙述错误的是( )
有关Fe-C-Nac1溶液构成的原电池中,叙述错误的是( )| A. | 铁片为负极,碳棒为正极 | |
| B. | 铁被腐蚀,碳棒上有氯气放出 | |
| C. | 碳棒附近的溶液可使酚酞变红 | |
| D. | 导线上有电流通过,电流方向是由碳极流向铁极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表里属于过渡元素的化合物 | |
| B. | 位于元素周期表里第ⅡA族元素的化合物 | |
| C. | 位于元素周期表里第ⅢA族元素的化合物 | |
| D. | 位于元素周期表里第ⅣA族元素的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 46g NO2和N2O4以任意比混合,所得混合气体中氧原子数2NA | |
| B. | 标准状况下,含NA个共价键的HF分子所占的体积约为22.4 L | |
| C. | 1mol Fe 与一定量的硝酸反应,转移的电子数为0.2NA~0.3NA | |
| D. | 2mol NO和1mol O2混合,在密闭容器中充分反应后,容器内的分子数小于2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若a=b,pH(NaX)>pH(NaY),则相同浓度时,酸性HX>HY | |
| B. | 若a=b,并测得溶液中c(X-)=c(Y-)+c(HY)(c(HY)≠0),则相同浓度时,酸性HX>HY | |
| C. | 若a>b,并测得溶液中c(HX)=c(HY),则可推出溶液中c(X-)>c(Y-),且相同浓度时,酸性HX>HY | |
| D. | 若两溶液等体积混合,测得溶液中c(X-)+c(Y-)+c(HX)+c(HY)=0.1 mol/L,则可推出a+b=0.2 mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com