
| A£® | CH3OHµÄČ¼ÉÕČČĪŖ192.9 kJ/mol | |
| B£® | CH3OH×Ŗ±ä³ÉH2µÄ¹ż³Ģ²»Ņ»¶ØŅŖĪüŹÕÄÜĮæ | |
| C£® | øł¾Ż¢Ł¢ŚĶĘÖŖ·“Ó¦£ŗH2O£Øg£©ØTH2£Øg£©+$\frac{1}{2}$O2£Øg£©”÷H=+241.9 kJ/mol | |
| D£® | øł¾Ż¢ŚĶĘÖŖ·“Ó¦£ŗCH3OH£Øl£©+$\frac{1}{2}$O2£Øg£©ØTCO2£Øg£©+2H2£Øg£©µÄ”÷H£¾-192.9 kJ/mol |
·ÖĪö A”¢Č¼ÉÕČČŹĒŌŚ101kPĻĀ£¬1molæÉČ¼ĪļĶźČ«Č¼ÉÕÉś³ÉĪČ¶ØµÄŃõ»ÆĪļŹ±Ėł·Å³öµÄČČĮ棻
B”¢CH3OH×Ŗ±ä³ÉH2æÉŅŌĶعż·“Ó¦¢ŁĄ“ŹµĻÖ£¬Ņ²æÉŅŌĶعż·“Ó¦¢ŚĄ“ŹµĻÖ£»
C”¢øł¾ŻøĒĖ¹¶ØĀÉ£¬½«·“Ó¦¢Ł-¢ŚæɵĆH2O£Øg£©ØTH2£Øg£©+$\frac{1}{2}$O2£Øg£©£»
D”¢¶ŌÓŚ·ÅČČ·“Ó¦£¬·“Ó¦ĪļµÄÄÜĮæŌ½µĶ£¬·“Ó¦·Å³öµÄČČĮæŌ½ÉŁ£¬Ōņ”÷HŌ½“ó£®
½ā“š ½ā£ŗA”¢Č¼ÉÕČČŹĒŌŚ101kPĻĀ£¬1molæÉČ¼ĪļĶźČ«Č¼ÉÕÉś³ÉĪČ¶ØµÄŃõ»ÆĪļŹ±Ėł·Å³öµÄČČĮ棬¼“HŌŖĖŲŅŖ×Ŗ»ÆĪŖŅŗĢ¬Ė®£¬¹Ź¼×“¼µÄČ¼ÉÕČČ²»ŹĒ192.9KJ/mol£¬¹ŹA“ķĪó£»
B”¢CH3OH×Ŗ±ä³ÉH2æÉŅŌĶعż·“Ó¦¢ŁĄ“ŹµĻÖ£¬Ņ²æÉŅŌĶعż·“Ó¦¢ŚĄ“ŹµĻÖ£¬¶ų·“Ó¦¢ŚĪŖ·ÅČČ·“Ó¦£¬¹Ź¼×“¼×Ŗ±äĪŖĒāĘų²»Ņ»¶ØŅŖĪüŹÕÄÜĮ棬¹ŹBÕżČ·£»
C”¢øł¾ŻøĒĖ¹¶ØĀÉ£¬½«·“Ó¦¢Ł-¢ŚæÉµĆ£ŗH2O£Øg£©ØTH2£Øg£©+$\frac{1}{2}$O2£Øg£©”÷H=49.0KJ/mol-£Ø-192.9KJ/mol£©=+241.9KJ/mol£¬¹ŹCÕżČ·£»
D”¢1molCH3OH£Øl£©µÄÄÜĮæµĶÓŚ1molCH3OH£Øg£©Ėł¾ßÓŠµÄÄÜĮ棬¶ų¶ŌÓŚ·ÅČČ·“Ó¦£¬·“Ó¦ĪļµÄÄÜĮæŌ½µĶ£¬·“Ó¦·Å³öµÄČČĮæŌ½ÉŁ£¬Ōņ”÷HŌ½“󣬹Ź·“Ó¦CH3OH£Øl£©+$\frac{1}{2}$O2£Øg£©ØTCO2£Øg£©+2H2£Øg£©µÄ”÷H£¾-192.9 kJ/mol£¬¹ŹDÕżČ·£®
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éĮĖČČ»Æѧ·½³ĢŹ½µÄ·ÖĪöÓ¦ÓĆ£¬ÕĘĪÕøĒĖ¹¶ØĀɵÄŌĖÓĆ”¢·“Ó¦ČČµÄ“óŠ”±Č½ĻŗĶĪļÖŹÄÜĮæµÄ±ä»ÆÅŠ¶ĻŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | c£ØNH4+£©=c£ØCl-£©µÄNH4ClŗĶ°±Ė®µÄ»ģŗĻČÜŅŗ | |
| B£® | c£ØH+£©=1.0”Į10-7mol•L-1µÄČÜŅŗ | |
| C£® | pH=7µÄČÜŅŗ | |
| D£® | ŹŅĪĀĻĀ½«pH=3µÄĖįÓėpH=11µÄ¼īµČĢå»ż»ģŗĻŗóµÄČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ĻĀĮŠøÅÄīÖ®¼äµÄ“ÓŹō¹ŲĻµÕżČ·µÄŹĒ£Ø””””£©
ĻĀĮŠøÅÄīÖ®¼äµÄ“ÓŹō¹ŲĻµÕżČ·µÄŹĒ£Ø””””£©| Ń”Ļī | A | B | C | D |
| ¢Ł | “æ¼ī | ½šŹōŃõ»ÆĪļ | ŗĻ½š | ĶĀĢ |
| ¢Ś | ¼ī | ¼īŠŌŃõ»ÆĪļ | »ģŗĻĪļ | ¼ī |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŃÖŖ H+£Øaq£©+OH-£Øaq£©ØTH2O£Øl£©”÷H=-57.3 kJ•mol-1£¬Ōņ H2SO4ŗĶBa£ØOH£©2·“Ó¦µÄ·“Ó¦ČČ”÷H=2”Į£Ø-57.3£©kJ•mol-1 | |
| B£® | ĘĻĢŃĢĒµÄČ¼ÉÕČČŹĒ2800 kJ•mol-1£¬Ōņ $\frac{1}{2}$C6H12O6£Øs£©+3O2£Øg£©ØT3CO2£Øg£©+3H2O£Øl£©”÷H=-1400kJ•mol-1 | |
| C£® | H2£Øg£©µÄČ¼ÉÕČČŹĒ285.8 kJ•mol-1£¬Ōņ 2H2O£Øg£©ØT2H2£Øg£©+O2£Øg£©”÷H=+571.6 kJ•mol-1 | |
| D£® | Č¼ĮĻµē³ŲÖŠ½«¼×“¼ÕōĘų×Ŗ»ÆĪŖĒāĘųµÄČČ»Æѧ·½³ĢŹ½ŹĒ CH3OH£Øg£©+$\frac{1}{2}$O2£Øg£©ØTCO2£Øg£©+2H2£Øg£©”÷H=-192.9 kJ•mol-1£¬Ōņ CH3OH£Øg£©µÄČ¼ÉÕČČĪŖ 192.9 kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
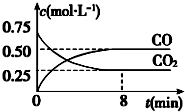 Ņ»¶ØĢõ¼žĻĀĢśæÉŅŌŗĶCO2·¢Éś·“Ó¦£ŗFe£Øs£©+CO2£Øg£© FeO£Øs£©+CO£Øg£©”÷H£¾0£¬1100”ꏱ£¬ĻņijĆܱÕČŻĘ÷ÖŠ¼ÓČė×ćĮæĢś·Ū²¢³äČėŅ»¶ØĮæµÄCO2ĘųĢ壬·“Ó¦¹ż³ĢÖŠCO2ŗĶCOµÄÅضČÓėŹ±¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®
Ņ»¶ØĢõ¼žĻĀĢśæÉŅŌŗĶCO2·¢Éś·“Ó¦£ŗFe£Øs£©+CO2£Øg£© FeO£Øs£©+CO£Øg£©”÷H£¾0£¬1100”ꏱ£¬ĻņijĆܱÕČŻĘ÷ÖŠ¼ÓČė×ćĮæĢś·Ū²¢³äČėŅ»¶ØĮæµÄCO2ĘųĢ壬·“Ó¦¹ż³ĢÖŠCO2ŗĶCOµÄÅضČÓėŹ±¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®| ¼× | ŅŅ | |
| Įæ | 3mo””Fe”¢ mo””CO | mo””FeO”¢ 3mo””CO |
| COÅØ¶Č£Ømo•-1£© | c1 | c |
| COĢå»ż·ÖŹż | ¦Õ1 | ¦Õ |
| ĢåĻµŃ¹Ēæ£ØPa£© | p1 | p |
| ĘųĢ¬×Ŗ»ÆĀŹ | ¦Į1 | ¦Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀĢÉ«»ÆѧµÄŗĖŠÄŹĒÓ¦ÓĆ»ÆѧŌĄķ¶Ō»·¾³ĪŪČ¾½ųŠŠÖĪĄķ | |
| B£® | PM2.5±ķĆ껿“ó£¬ÄÜĪüø½“óĮæµÄÓŠ¶¾ÓŠŗ¦ĪļÖŹ£¬¶ŌČĖµÄ·Ī¹¦ÄÜŌģ³ÉŗÜ“óĪ£ŗ¦ | |
| C£® | ¶žŃõ»Æ¹č¹ć·ŗÓ¦ÓĆÓŚĢ«ŃōÄܵē³Ų”¢¼ĘĖ滜Š¾Ę¬ | |
| D£® | Ęū³µĪ²ĘųÖŠŗ¬ÓŠ“óĮæ“óĘųĪŪČ¾Īļ£¬ÕāŹĒĘūÓĶ²»ĶźČ«Č¼ÉÕŌģ³ÉµÄ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉÕ± | B£® | ²£Į§°ō | C£® | ČŻĮæĘæ | D£® | ·ÖŅŗĀ©¶· |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com