
| A. | 少量金属钠保存在煤油中 | |
| B. | 保存硫酸亚铁溶液时,要向其中加入少量硫酸和铁粉 | |
| C. | 浓硝酸用带橡胶塞的细口、棕色试剂瓶盛放,并贮存在阴凉处 | |
| D. | 试剂瓶中的液溴可用水封存,防止溴挥发 |
分析 A.钠易与空气中的氧气、水反应;
B.硫酸亚铁易被氧化为硫酸铁;
C.浓硝酸有强氧化性;
D.溴单质易挥发.
解答 解:A.钠易与空气中的氧气、水等反应,与煤油不反应,且密度比煤油大,可保存在煤油中,故A正确;
B.硫酸亚铁易被氧化为硫酸铁,常加入少量铁粉防止亚铁离子被氧化,加入硫酸防止其水解,故B正确;
C.浓硝酸有强氧化性,会腐蚀橡胶塞,故C错误;
D.溴单质易挥发,溴的密度比水大,溴微溶于水.为防止液溴挥发,所以用水密封,故D正确.
故选C.
点评 本题考查较为综合,涉及药瓶的保存,侧重于学生的分析能力和实验能力的考查,为高频考点,注意药品的保存取决于物质的性质,学习中注意相关基础知识的积累,难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都减小 | B. | 都增大 | C. | v1减小v2增大 | D. | v1增大v2减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热的浓盐酸可以除去烧瓶内残留的MnO2 | |
| B. | 过量的铜与浓硝酸反应会有一氧化氮生成 | |
| C. | 稀硝酸可除去试管内壁的银镜 | |
| D. | 白磷在空气中加热到一定温度能转化成红磷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓氢氧化钠溶液-浓盐水 | B. | 稀碳酸钠溶液-浓盐水 | ||
| C. | 浓盐酸-浓氨水 | D. | 稀硫酸-浓氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火,用泡沫灭火器灭火 | |
| B. | 苯酚不慎沾在皮肤上,应马上用NaOH溶液清洗 | |
| C. | 当不慎在皮肤上沾上浓硫酸时,应立即用抹布擦拭,然后再用大量水冲洗 | |
| D. | 误食氯化钡溶液,应立即服用大量硫酸铜溶液解毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
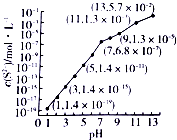 研究硫元素及其化合物的性质具有重要意义.
研究硫元素及其化合物的性质具有重要意义.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com