
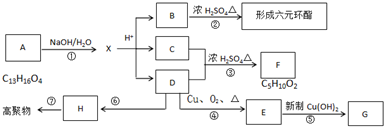
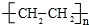 .C与乙醇在浓硫酸作用下生成F,由F的分子式可知,应发生酯化反应,故C为CH3CH2COOH,F为CH3CH2COOCH2CH3.A发生水解生成乙醇、乙酸和B,A、B属于芳香族化合物,且B不能使FeCl3溶液显紫色,B不含酚羟基,含有羧基、醇羟基,B可以形成六元环化合物,结合A的分子式可知B为
.C与乙醇在浓硫酸作用下生成F,由F的分子式可知,应发生酯化反应,故C为CH3CH2COOH,F为CH3CH2COOCH2CH3.A发生水解生成乙醇、乙酸和B,A、B属于芳香族化合物,且B不能使FeCl3溶液显紫色,B不含酚羟基,含有羧基、醇羟基,B可以形成六元环化合物,结合A的分子式可知B为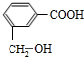 ,据此解答.
,据此解答.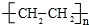 .C与乙醇在浓硫酸作用下生成F,由F的分子式可知,应发生酯化反应,故C为CH3CH2COOH,F为CH3CH2COOCH2CH3.A发生水解生成乙醇、乙酸和B,A、B属于芳香族化合物,且B不能使FeCl3溶液显紫色,B不含酚羟基,含有羧基、醇羟基,B可以形成六元环化合物,结合A的分子式可知B为
.C与乙醇在浓硫酸作用下生成F,由F的分子式可知,应发生酯化反应,故C为CH3CH2COOH,F为CH3CH2COOCH2CH3.A发生水解生成乙醇、乙酸和B,A、B属于芳香族化合物,且B不能使FeCl3溶液显紫色,B不含酚羟基,含有羧基、醇羟基,B可以形成六元环化合物,结合A的分子式可知B为 ,
,| 浓硫酸 |
| △ |
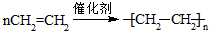 ,
,| 浓硫酸 |
| △ |
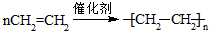 ;
; )同分异构体有多种,符合下列条件的同分异构体:①是苯环的二元取代物 ②遇FeCl3溶液显紫色,含有酚羟基,③遇Na2CO3溶液反应产生无色气体,含有羧基,而B的取代基为-COOH和-CH2OH,根据条件变换取代基,得出同分异构体的结构简式为:
)同分异构体有多种,符合下列条件的同分异构体:①是苯环的二元取代物 ②遇FeCl3溶液显紫色,含有酚羟基,③遇Na2CO3溶液反应产生无色气体,含有羧基,而B的取代基为-COOH和-CH2OH,根据条件变换取代基,得出同分异构体的结构简式为: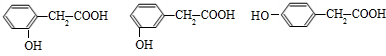 ,
,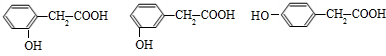 任意一种.
任意一种.


科目:高中化学 来源: 题型:
| A、使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+ |
| B、使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl- |
| C、碳酸氢钠溶液:K+、SO42-、Cl-、H+ |
| D、c(H+)=10-12 mol?L-1的溶液:K+、Ba2+、Cl-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:

 )
)查看答案和解析>>
科目:高中化学 来源: 题型:
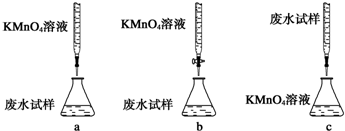
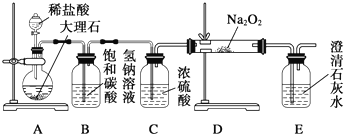
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室里有一瓶试剂的标签部分被腐蚀,如图所示,仅知该试剂是只含短周期元素的纯净物.某同学设计实验探究该试剂成分,实验现象和结论都正确的是( )
实验室里有一瓶试剂的标签部分被腐蚀,如图所示,仅知该试剂是只含短周期元素的纯净物.某同学设计实验探究该试剂成分,实验现象和结论都正确的是( )| A、取该样品加入足量的硝酸钡溶液和稀盐酸,产生白色沉淀,则该样品的成分一定是硫酸钠 |
| B、取该样品溶于水,测得溶液pH=10,将溶液放置在空气中,一段时间后再测定溶液pH=7,该样品可能是亚硫酸钠 |
| C、取该样品溶于水,加入足量稀硫酸,将产生气体通入品红溶液,品红溶液褪色,加热溶液变红色,则样品成分是Na2S |
| D、若样品成分是硅酸钠(Na2SiO3),溶于水,滴加盐酸至过量,先生成白色沉淀,后沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 试剂 | 分离方法 | |
| ① | 乙酸乙酯(乙酸) | 饱和Na2CO3溶液 | 分液 |
| ② | 溴乙烷(乙醇) | HBr | 分液 |
| ③ | 乙醇(水) | 生石灰 | 蒸馏 |
| ④ | 苯(苯酚) | 浓溴水 | 过滤 |
| A、①② | B、①③ | C、只有③ | D、③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com