
分析 (1)由①C(s)+CO2(g)?2CO(g) K1
②CO(g)+H2O(g)?CO2(g)+H2(g) K2
结合盖斯定律可知,①+②得到C(s)+H2O(g)?CO(g)+H2(g);
(2)25℃时Kw=10-14,溶液pH=10,可知碱过量,设酸的体积为x,强碱体积为y,则$\frac{0.01mol/L×x-y×0.001mol/L}{x+y}$=10-4mol/L.
解答 解:(1)由①C(s)+CO2(g)?2CO(g) K1
②CO(g)+H2O(g)?CO2(g)+H2(g) K2
结合盖斯定律可知,①+②得到C(s)+H2O(g)?CO(g)+H2(g),则K3=K1×K2,
故答案为:K1×K2;
(2)25℃时Kw=10-14,溶液pH=10,可知碱过量,设酸的体积为x,强碱体积为y,则$\frac{0.01mol/L×x-y×0.001mol/L}{x+y}$=10-4mol/L,
解得x:y=9:1,
故答案为:9:1.
点评 本题考查化学平衡的计算,为高频考点,把握K与化学计量数的关系、酸碱混合的计算为解答的关键,侧重分析与计算能力的考查,注意盖斯定律的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 2:1 | B. | 1:2 | C. | 4:1 | D. | 1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
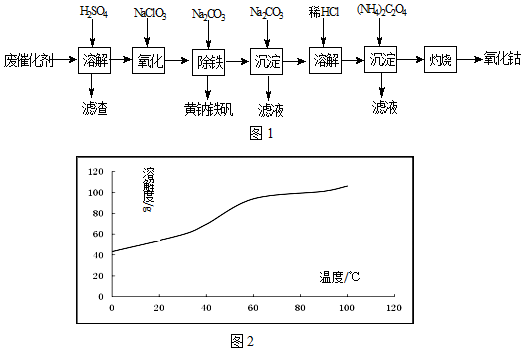
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
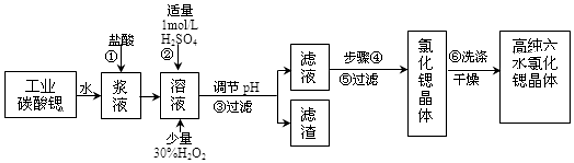
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 |
| 沉淀完全的pH | 3.7 | 9.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
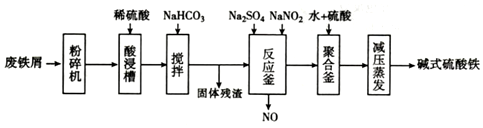
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
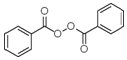 也被禁用. 下面是一种以苯为原料合成过氧化苯甲酰的流程:
也被禁用. 下面是一种以苯为原料合成过氧化苯甲酰的流程: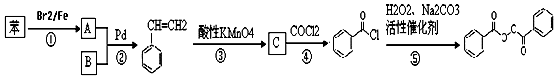
 $\stackrel{Pd}{→}$
$\stackrel{Pd}{→}$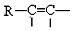
 ;
;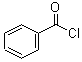 +H2O2$\frac{\underline{\;催化剂\;}}{碳酸钠}$
+H2O2$\frac{\underline{\;催化剂\;}}{碳酸钠}$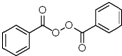 +2HCl;
+2HCl;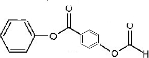 、
、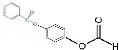 ;
; ;
; 的流程,无机物任选,注明反应条件.
的流程,无机物任选,注明反应条件.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com