
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:
①X元素原子价电子排布式为ns2np2,且原子半径是同族元素中最小的。
②Y元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的电
子排布中,p轨道上只有1个未成对电子。
③Z+与Y 2-具有相同的电子层结构;
请回答:
(1)Z2Y2的电子式为 ,含有的化学键类型为 ,Z2Y2为 晶体。
(2)X、Y、Z三种元素所形成的常见化合物的名称为 ;XY2的结构式为 ,分子的立体构型为 。
(3)X、Y、Z、W四种元素所形成的单质中,熔点最高、硬度最大的是 (填名称);晶体ZW的熔点比晶体XW4明显高的原因是 。

(4)ZW晶体的结构示意图如图。已知:ZW晶体的密度为ρ,摩尔质量为M,阿伏伽德罗常数为NA,则ZW晶体中两个最近的Z离子中心间的距离d可以表示为d= 。
(每空2分). (1)  离子键、非极性共价键, 离子
离子键、非极性共价键, 离子
(2) 碳酸钠,,直线形 
(3) 金刚石;
NaCl为离子晶体而CCl4为分子晶体 (4)
【解析】
试题分析:X元素原子价电子排布式为ns2np2,且原子半径是同族元素中最小的,所以X应该是第ⅣA族元素的碳元素。Y元素是地壳中含量最多的元素,因此Y是氧元素。W元素的电负性略小于Y元素,在W原子的电子排布中,p轨道上只有1个未成对电子,且W的原子序数大于氧元素的,所以W是氯元素。Z+与Y 2-具有相同的电子层结构,则Z是钠元素。在氯化钠晶胞中含有4个钠离子和4个氯离子,设晶胞的边长是x,则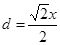 。又因为
。又因为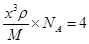 ,解得d=
,解得d= 。
。
考点:考查元素周期表的结构、化学键、电子式、结构式以及分子空间构型的判断和晶体类型的有关计算
点评:该题是高考中的常见考点,属于基础性试题的考查。试题综合性强,难易适中,侧重对学生基础知识的巩固和训练,有利于培养学生的逻辑推理能力和抽象思维能力,提高学生灵活运用基础知识解决实际问题的能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力,考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。


科目:高中化学 来源:2013-2014学年福建省龙岩市高三毕业班教学质量检查理综化学试卷(解析版) 题型:填空题
I.短周期元素X、Y、Z、W在元素周期表中相对位置如图所示,其中Y所处的周期序数与族序数相等。按要求回答下列问题:

(1)写出X的原子结构示意图_______________。
(2)列举一个事实说明W非金属性强于Z: _______________(用化学方程式表示)。
(3)含Y的某种盐常用作净水剂,其净水原理是__________(用离子方程式表示)。
II.运用所学化学原理,解决下列问题:
(4)已知:Si+2NaOH+H2O=Na2SiO3+2H2。某同学利用单质硅和铁为电极材料设计原电池(NaOH为电解质溶液),该原电池负极的电极反应式为_________________。
(5)已知:①C(s)+ O2(g)=CO2(g)?  H=a kJ· mol-1;②CO2(g) +C(s)=2CO(g)
H=a kJ· mol-1;②CO2(g) +C(s)=2CO(g)  H=b kJ· mol-1;③Si(s)+ O2(g)=SiO2(s)?
H=b kJ· mol-1;③Si(s)+ O2(g)=SiO2(s)?  H=c kJ· mol-1。工业上生产粗硅的热化学方程式为____________。
H=c kJ· mol-1。工业上生产粗硅的热化学方程式为____________。
(6)已知:CO(g)+H2O(g) H2(g) + CO2(g)。右表为该反应在不同温度时的平衡常数。则:该反应的
H2(g) + CO2(g)。右表为该反应在不同温度时的平衡常数。则:该反应的 H________0(填“<”或“>”);500℃时进行该反应,且CO和H2O起始浓度相等,CO平衡转化率为_________。
H________0(填“<”或“>”);500℃时进行该反应,且CO和H2O起始浓度相等,CO平衡转化率为_________。

查看答案和解析>>
科目:高中化学 来源:2010-2011学年江西省吉安市高三第三次模拟考试(理综)化学部分 题型:填空题
X、Y、Z、Q、W为按原予序数由小到大排列的五种短周期元素。已知:①X与Q处于同一主族,其原子价电子排布式都为ns2np2,且X原子半径小于Q;②Y元素是地壳中含量最多的元素;W元素的电负性路小于Y元素,在W原子的价电子排布式中,p轨道上只有1个未成对电子;③Z元素的电离能数据见下表(kJ·mol-1)
|
I1 |
I2 |
I3 |
I4 |
… |
|
496 |
4562 |
6912 |
9540 |
… |
请回答:
(1)XY2分子的空间构型为 。
(2)QX的晶体结构与金刚石的相似,微粒间存在的作用力是 。
(3)晶体ZW的熔点比晶体XW4明显高的原因是 。
(4)XY2在高温高压下所形成的晶胞如图所示。该晶体的类型属于 (选填“分子”、“原子”、“离子”或“金属”)漏体,该晶体中X原子的杂化形式为___ 。

(5)氧化物MO的电子总数与QX的相等,则M为 。(填元素符号);MO是优良的耐高温材料,其晶体结构与ZW晶体结构相似,MO的熔点比CaO的高,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素。已知①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物。
请回答:
(1)Z2Y的化学式是 ,X2Y2的电子式 ,Z2Y2与X2Y反应的化学方程式是 .
(2)如图所示装置,两玻璃管中盛满滴有酚酞的ZW的饱和溶液,C(I)、C(II)为多孔石墨电极。接通S1后,C(I)附近溶液变红,两玻璃管中有气体聚集。此时C(I)为 极,电极反应式为 。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2电流表的指针发生偏转。此时C(II)为 极, 电极反应式为 。

(3)铜屑放入稀硫酸不发生反应,若在稀硫酸中加入X2Y2,铜屑可逐渐溶解,该反应的离子方程式是: 。若该方程式同时为一套原电池装置的总反应式,则该原电池负极反应式为 ,正极反应式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(08福州八中质检)X、Y、Z、W为按原子序数由小到大排列的四种短周期元素。已知①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;
②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物。
请回答:
(1)Z2Y的化学式是 ,X2Y2的电子式 ,Z2Y2与X2Y反应的化学方程式是 .
(2)如右图所示装置,两玻璃管中盛满滴有酚酞的
ZW的饱和溶液,C(I)、C(II)为多孔石墨电极。
接通S1后,C(I)附近溶液变红,两玻璃管中有
气体聚集。此时C(I)为 极,电极反应式为
。
一段时间后(两玻璃管中液面未脱离电极),断
开S1,接通S2电流表的指针发生偏转。此时
C(II)为 极, 电极反应式为
。
(3)铜屑放入稀硫酸不发生反应,若在稀硫酸中加入
X2Y2,铜屑可逐渐溶解,该反应的离子方程式是:
。若该方程式同时为一套原电池装置的总
反应式,则该原电池负极反应式为 ,正极反应式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z是四种常见的短周期元素,其原子序数依次增大。原子半径关系按 X、Y、Z 、W依次减小。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强。
(1)X位于元素周期表中第 周期第 族;X和W形成含有非极性键化合物的电子式 。
(2)X的单质和Y的单质相比,熔点较高的是 (写名称);Z的气态氢化物和溴化氢相比,较稳定的是 (写化学式)。
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是 。
(4)在25?C、101 kPa下,已知Y的气态化物在氧气中完全燃烧后恢复至原状态,平均每转移1mol 电子放热190.0kJ,该反应的热化学方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com