
| A. | 原子最外层只有两个电子的元素都在第ⅡA族 | |
| B. | 人们通常在过渡元素中寻找催化剂和耐高温、耐腐蚀的合金材料 | |
| C. | 共价化合物中可能含有离子键 | |
| D. | 水溶液能导电的化合物都是离子化合物 |
分析 A、氦原子核外有2个电子处于零族,一般性质相似处于同一族;
B、优良的催化剂和耐高温、耐腐蚀的合金材料大多属于过渡元素;
C、共价化合物中如果含有离子键,就不是共价化合物,而是离子化合物;
D、氯化氢水溶液能导电,但氯化氢是共价化合物.
解答 解:A、氦原子核外有2个电子,处于零族,故A错误;
B、优良的催化剂和耐高温、耐腐蚀的合金材料大多属于过渡元素,故B正确;
C、共价化合物中如果含有离子键,就不是共价化合物,而是离子化合物,故C错误;
D、氯化氢水溶液能导电,但氯化氢是共价化合物,故D错误;
故选B.
点评 本题考查元素周期表及元素周期律,为高频考点,把握元素在周期表的位置、元素的性质及变化规律为解答的关键,题目难度不大.


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:解答题
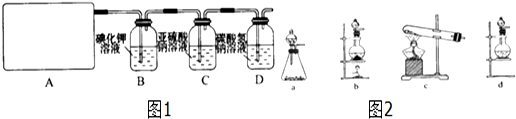
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入苯使之反应 | B. | 加入KI溶液 | ||
| C. | 加入较大量NaOH溶液后静置分液 | D. | 加入较大量的CCl4萃取静置后分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,23g NO2中含有NA个O原子 | |
| B. | 16g CH4中含有NA个C-H共价键 | |
| C. | 标准状态下,2.24L水中所含的分子数为0.1NA | |
| D. | 在0.1mol/L AlCl3溶液中所含的Cl- 的个数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2通入BaCl2溶液中无明显现象,说明碳酸的酸性比盐酸弱 | |
| B. | 氯水加入稀盐酸和AgNO3溶液产生白色沉淀,说明有氯水中有Cl-存在 | |
| C. | 常温下,Cu片投入到浓硫酸中不反应,因为浓硫酸使Cu产生钝化现象 | |
| D. | 浓硫酸具有脱水性,因而能使胆矾失去结晶水由蓝色变白色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 达到化学平衡时,υ正(NH3)=υ逆(H2O) | |
| B. | 达到化学平衡时,4υ (O2)=5υ (NO) | |
| C. | 若单位时间内生成x mol NO的同时,也消耗x mol NH3 | |
| D. | 若单位时间内生成4 mol NO的同时,也生成4 mol NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由二氧化碳和氧气组成的混合气体共有NA个分子,其中氧原子数为2NA | |
| B. | 1mol铜与足量稀硝酸反应可产生NO分子$\frac{2}{3}$NA个. | |
| C. | 12g金刚石中含有共价键数为4NA | |
| D. | 1L1mol/L硫酸铝溶液中阴阳离子总数大于5NA. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25g质量分数68%的H2O2水溶液中含氧原子数目为NA | |
| B. | 0.1mol•L-1 NH4Cl溶液中含有NH4+的数目小于0.1NA | |
| C. | 100mL 12mol•L-1 的浓HNO3与过量Cu反应转移电子的数目为0.6NA | |
| D. | 标准状况下,11.2L由C2H4和C3H4 组成的混合气体中含有氢原子的数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
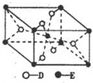
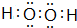 ,E的基态原子的外围电子排布式为3d24s2.
,E的基态原子的外围电子排布式为3d24s2.| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com