
分析 CH3COOH是弱电解质,部分电离生成CH3COO-、H+;
(1)加入冰醋酸,醋酸浓度增大平衡向正反应方向移动;
(2)浓度越小其电离程度越大;但其电离增大程度小于溶液体积增大程度;
(3)HCl电离出的氢离子抑制醋酸电离;
(4)加入氯化钠溶液相当于稀释醋酸,促进醋酸电离.
解答 解:CH3COOH是弱电解质,部分电离生成CH3COO-、H+,电离方程式为CH3COOH?CH3COO-+H+,
故答案为:CH3COOH?CH3COO-+H+;
(1)加入冰醋酸,醋酸浓度增大平衡向正反应方向移动,导致溶液中c(H+)增大,
故答案为:向电离方向移动;增大;
(2)浓度越小其电离程度越大,所以加水稀释促进醋酸电离,平衡向电离方向移动;但其电离增大程度小于溶液体积增大程度,导致溶液中c(H+)减小,
故答案为:向电离方向移动;减小;
(3)HCl电离出的氢离子抑制醋酸电离,所以抑制醋酸电离,则醋酸向离子结合成分子的方向移动,但溶液中c(H+)增大,
故答案为:向离子结合成分子的方向移动;增大;
(4)加入氯化钠溶液相当于稀释醋酸,促进醋酸电离,则醋酸向电离方向移动,因为醋酸电离增大程度小于溶液体积增大程度,所以c(H+)减小,故答案为:向电离方向移动;减小.
点评 本题考查弱电解质的电离,为高频考点,明确弱电解质电离特点及电离影响因素是解本题关键,知道弱电解质电离程度与其浓度关系,题目难度不大.


科目:高中化学 来源: 题型:实验题
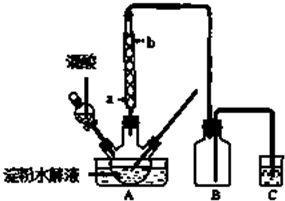
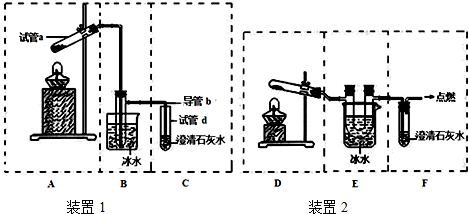
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
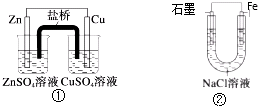
| A. | 装置②中的Fe发生析氢腐蚀 | |
| B. | 装置①中,Zn为负极,发生还原反应 | |
| C. | 装置①中,盐桥中的K+移向CuSO4溶液 | |
| D. | 装置②中电子由Fe流向石墨,然后再经溶液流向Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
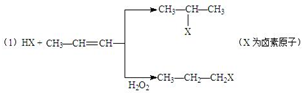
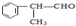 的物质,该物质是一种香料.
的物质,该物质是一种香料.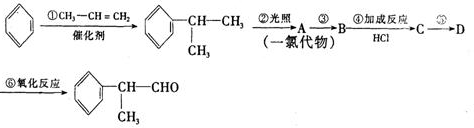
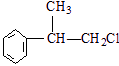 、
、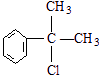 .
.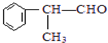 的官能团的名称醛基.
的官能团的名称醛基.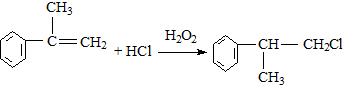 .
.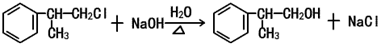 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
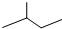
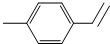 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部可以 | B. | 仅②不可以 | C. | 仅②④不可以 | D. | 仅③可以 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com