
| A、(2a-1.6)g |
| B、2(a-1.6)g |
| C、(a-1.6)g |
| D、3.2 g |


科目:高中化学 来源: 题型:
| A、150 mL |
| B、200 mL |
| C、450 mL |
| D、无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶质 | Na2CO3 | NaClO | NaHCO3 | NaHSO3 |
| pH | 11.6 | 10.3 | 9.7 | 4.0 |
| A、常温下,HSO3?的水解能力强于其电离能力 |
| B、常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH依次升高 |
| C、Na2CO3溶液中存在以下关系:c(Na+)+c(H+)=c(CO32?)+c(HCO3?)+c(OH?) |
| D、向氯水中加入少量NaHCO3固体,不能增大HClO的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
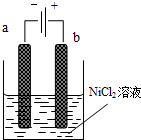 三氧化二镍(Ni2O3)可用于制造高能电池.一种制备Ni2O3的方法是电解NiCl2得Ni3+,再将Ni3+经一系列反应后转化为Ni2O3.其电解制备过程如下:用NaOH调NiCl2溶液pH至7.5,加放适量硫酸钠后进行电解.电解过程中产生的Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍.如图为电解装置示意图,电解池两极用阳离子交换膜隔开.请回答下列问题:
三氧化二镍(Ni2O3)可用于制造高能电池.一种制备Ni2O3的方法是电解NiCl2得Ni3+,再将Ni3+经一系列反应后转化为Ni2O3.其电解制备过程如下:用NaOH调NiCl2溶液pH至7.5,加放适量硫酸钠后进行电解.电解过程中产生的Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍.如图为电解装置示意图,电解池两极用阳离子交换膜隔开.请回答下列问题:| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过滤、蒸发、结晶、溶解 |
| B、溶解、蒸发、过滤、结晶 |
| C、溶解、蒸发、结晶、过滤 |
| D、溶解、过滤、蒸发、结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 成分 | NaOH | Na2CO3 | H2O |
| 质量分数 | 90.4% | 3.8% | 5.8% |
| A、4.68 g |
| B、5.85 g |
| C、2.34 g |
| D、(2.34-a) g |
查看答案和解析>>
科目:高中化学 来源: 题型:
 能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.
能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com