
【题目】如图1,将2 mol SO2和1 mol O2混合置于体积可变的密闭容器中,在T1温度下发生如下反应:2SO2(g)+O2(g)![]() 2SO3(g);△H<0。当反应进行到时间 t0时达到平衡状态,测得混合气体的总物质的量为2.1 mol。 试回答:
2SO3(g);△H<0。当反应进行到时间 t0时达到平衡状态,测得混合气体的总物质的量为2.1 mol。 试回答:

(1)t0时SO3的物质的量为:____________,在图2中作出反应混合物中各组分气体的物质的量随反应进行到t0时的变化曲线____________;
(2)当反应进行到t1时间时(t1>t0),给上述反应容器加热到温度为T2 (T2>T1),反应在t3时(t3>t1)重新达到平衡状态,新平衡混合物中气体的总物质的量________2.1 mol(填“<”、“>”或“=”)。
(3)如图1所示,若起始时在容器中加入0.6 mol SO2、0.3 mol O2 ,保持温度不变,达到平衡状态后,SO3气体的体积分数与上述平衡相比__________(填“<”、“>”或“=”)。。
(4)V2O5是上述反应的催化剂,催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒氧化物;四价钒氧化物再被氧气氧化。写出该催化循环机理的化学方程式________,_______;
【答案】1.8mol  > = SO2+ V2O5=SO3+2VO2 4VO2+ O2=2V2O5
> = SO2+ V2O5=SO3+2VO2 4VO2+ O2=2V2O5
【解析】
(1)设达到平衡时生成SO3的物质的量为xmol;
2SO2 + O2![]() 2SO3
2SO3
起始 2 mol 1 mol 0
转化 xmol ![]() mol x mol
mol x mol
平衡 (2-x)mol (1-![]() ) mol x mol
) mol x mol
据题意:(2-x) mol+(1-![]() ) mol+x mol=2.1 mol,解得x=1.8。(2)正反应放热,升高温度平衡逆向移动;(3)恒温、恒压,若起始时在容器中加入0.6 mol SO2、0.3 mol O2 ,则新平衡与原平衡是等效平衡;(4)V2O5氧化SO2时,自身被还原为四价钒氧化物,SO2被氧化为SO3;四价钒氧化物再被氧气氧化为V2O5。
) mol+x mol=2.1 mol,解得x=1.8。(2)正反应放热,升高温度平衡逆向移动;(3)恒温、恒压,若起始时在容器中加入0.6 mol SO2、0.3 mol O2 ,则新平衡与原平衡是等效平衡;(4)V2O5氧化SO2时,自身被还原为四价钒氧化物,SO2被氧化为SO3;四价钒氧化物再被氧气氧化为V2O5。
(1)设达到平衡时生成SO3的物质的量为xmol;
2SO2 + O2![]() 2SO3
2SO3
起始 2 mol 1 mol 0
转化xmol ![]() mol x mol
mol x mol
平衡 (2-x)mol (1-![]() ) mol x mol
) mol x mol
据题意:(2-x) mol+(1-![]() ) mol+x mol=2.1 mol,解得x=1.8。
) mol+x mol=2.1 mol,解得x=1.8。
t0时SO3的物质的量为1.8mol,SO2 的物质的量由2变为0.2、O2的物质的量由1变为0.1、SO3的物质的量由0变为1.8,反应混合物中各组分气体的物质的量随反应进行到t0时的变化曲线为 ;(2)正反应放热,升高温度平衡逆向移动,所以新平衡混合物中气体的总物质的量>2.1 mol;(3)恒温、恒压,若起始时在容器中加入0.6 mol SO2、0.3 mol O2 ,则新平衡与原平衡是等效平衡;达到平衡状态后,SO3气体的体积分数与上述平衡相相等;(4)V2O5氧化SO2时,自身被还原为四价钒氧化物,SO2被氧化为SO3;四价钒氧化物再被氧气氧化为V2O5,根据得失电子守恒,反应方程式是SO2+ V2O5=SO3+2VO2 、 4VO2+ O2=2V2O5。
;(2)正反应放热,升高温度平衡逆向移动,所以新平衡混合物中气体的总物质的量>2.1 mol;(3)恒温、恒压,若起始时在容器中加入0.6 mol SO2、0.3 mol O2 ,则新平衡与原平衡是等效平衡;达到平衡状态后,SO3气体的体积分数与上述平衡相相等;(4)V2O5氧化SO2时,自身被还原为四价钒氧化物,SO2被氧化为SO3;四价钒氧化物再被氧气氧化为V2O5,根据得失电子守恒,反应方程式是SO2+ V2O5=SO3+2VO2 、 4VO2+ O2=2V2O5。


科目:高中化学 来源: 题型:
【题目】ⅡBⅥA族半导体纳米材料(如CdTe、CdSe、ZnSe、ZnS等)在光电子器件、太阳能电池以及生物探针等方面有广阔的前景。回答下列问题:
(1)基态锌(Zn)原子的电子排布式为[Ar]_____。
(2)“各能级最多容纳的电子数,是该能级原子轨道数的二倍”,支撑这一结论的理论是______(填标号)
a 构造原理 b 泡利原理 c 洪特规则 d 能量最低原理
(3)在周期表中,Se与As、Br同周期相邻,与S、Te同主族相邻。Te、As、Se、Br的第一电离能由大到小排序为_______。
(4)H2O2和H2S的相对分子质量相等,常温下,H2O2呈液态,而H2S呈气态,其主要原因是______;![]() 的中心原子杂化类型为_______,其空间构型为_______。
的中心原子杂化类型为_______,其空间构型为_______。
(5)ZnO具有独特的电学及光学特性,是一种应用广泛的功能材料。
①已知锌元素、氧元素的电负性分别为1.65、3.5,ZnO中化学键的类型为______。ZnO可以被NaOH溶液溶解生成[Zn(OH)4]2—,请从化学键角度解释能够形成该离子的原因。_______。

②一种ZnO晶体的晶胞如图所示。晶胞边长为a nm、阿伏加德罗常数的值为NA,其晶体密度为________g·cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电池在人类生产生活中具有十分重要的作用,其中锂离子电池与太阳能电池占有很大比重。太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置。其材料有单晶硅,还有铜、锗、镓、硒等化合物。
(1)基态亚铜离子中电子占据的原子轨道数目为____________。
(2)若基态硒原子价层电子排布式写成4s24px24py2,则其违背了____________。
(3)下图表示碳、硅和磷元素的四级电离能变化趋势,其中表示磷的曲线是_______(填标号)。

(4)元素X与硅同主族且原子半径最小,X形成的最简单氢化物Q的电子式为_____,该分子其中心原子的杂化类型为_____。写出一种与Q互为等电子体的离子______。
(5)与镓元素处于同一主族的硼元素具有缺电子性。自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作Na2B4O7·10H2O,实际上它的结构单元是由两个H3BO3和两个[B(OH)4]-缩合而成的双六元环,应该写成Na2[B4O5(OH)4]8H2O.其结构如图所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是__________(填选项字母)。

A 离子键 B 共价键 C 金属键 D 范德华力 E 氢键
(6)GaAs的熔点为1238℃,密度为ρg·cm3,其晶胞结构如图所示。已知GaAs与GaN具有相同的晶胞结构,则二者晶体的类型均为____,GaAs的熔点____(填“高于”或“低于”)GaN。Ga和As的摩尔质量分别为MGa gmol1和MAs gmol1,原子半径分别为rGa pm和rAs pm,阿伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是人类赖以生存和发展的重要物质基础,常规能源的合理利用和新能源的合理开发是当今社会面临的严峻课题,回答下列问题:
(1)乙醇是未来内燃机的首选环保型液体燃料。2.0g乙醇完全燃烧生成液态水放出59.43kJ的热量,则乙醇燃烧的热化学方程式为__________________________________________________________ 。
(2)由于C3H8(g)![]() C3H6(g)+H2(g) ΔH=+bkJ·mol-1(b>0)的反应中,反应物具有的总能量________(填“大于”“等于”或“小于”)生成物具有的总能量,那么在化学反应时,反应物就需要________(填“放出”或“吸收”)能量才能转化为生成物。
C3H6(g)+H2(g) ΔH=+bkJ·mol-1(b>0)的反应中,反应物具有的总能量________(填“大于”“等于”或“小于”)生成物具有的总能量,那么在化学反应时,反应物就需要________(填“放出”或“吸收”)能量才能转化为生成物。
(3)关于用水制取二次能源氢气,以下研究方向不正确的是(________)
A.组成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二次能源
B.设法将太阳光聚焦,产生高温,使水分解产生氢气
C.寻找高效催化剂,使水分解产生氢气,同时释放能量
D.寻找特殊催化剂,用于开发廉价能源,以分解水制取氢气
(4)已知下列两个热化学方程式:
A、2H2(g)+O2(g)![]() 2H2O(l) △H=-571.6kJ·mol-1
2H2O(l) △H=-571.6kJ·mol-1
B、C3H8(g)+5O2(g)![]() 3CO2(g)+4H2O(l) △H=-2220kJ·mol-1
3CO2(g)+4H2O(l) △H=-2220kJ·mol-1
其中,能表示燃烧热的热化学方程式为__________,其燃烧热△H=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法中错误的是( )

A. 由红外光谱可知,该有机物中至少有三种不同的化学键
B. 由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子
C. 仅由其核磁共振氢谱无法得知其分子中的氢原子总数
D. 若A的化学式为C2H6O,则其结构简式为CH3—O—CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食品安全一直是社会关注的话题。过氧化苯甲酰(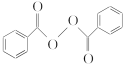 )过去常用作面粉增白剂,但目前已被禁用。合成过氧化苯甲酰的流程图如下:
)过去常用作面粉增白剂,但目前已被禁用。合成过氧化苯甲酰的流程图如下:
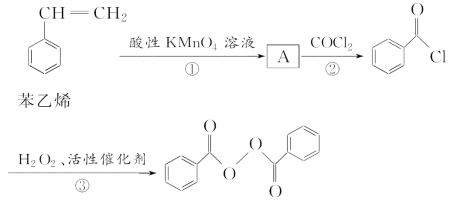
请回答下列问题:
(1)A的结构简式为________________;②的反应类型为________________。
(2)写出反应③的化学方程式:_________________________________________
过氧化苯甲酰在酸性条件下水解的化学方程式为__________________________________。
(3)下列有关苯乙烯的说法正确的是______(填字母)。
A.苯乙烯能使溴水褪色 B.苯乙烯存在一种同分异构体,其一氯代物仅有一种
C.苯乙烯分子中8个碳原子可能共平面 D.苯乙烯、庚烷燃烧耗氧量肯定相等
(4)写出一个符合下列要求的过氧化苯甲酰的同分异构体的结构简式______________。
①分子中不含碳碳双键或三键;
②分子中只含有一种含氧官能团;
③核磁共振氢谱有3组峰,其峰面积之比为1∶2∶2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知HA为一元酸,常温下向20mL0.01mol/L的HA溶液中滴加0.01mol/L的NaOH溶液,测得溶液pH与所加NaOH溶液体积关系如图所示。下列说法不正确的是

A. 常温下,该酸的电离常数K=10-5.6
B. 该测定过程中不可以选择甲基橙为指示剂
C. 滴定至①处时,溶液中离子浓度关系为:c(A-)>c(Na+)>c(H+)>c(OH-)
D. 由①到③过程中,水的电离程度先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磁性材料产业是21世纪各国竞相发展的高科技支柱产业之一,磁性材料广泛用于电子信息、军事技术等领域。碳酸锰主要用于制备软磁铁氧体,工业上用氯化铵焙烧锰矿粉制备高纯度碳酸锰的工艺流程如下:

已知:①锰矿粉的主要成分是MnCO3,还含少量Fe、Al、Ca、Mg等元素。
②相关金属Mn+离子c(Mn+) ═ 0.1 mol L -1形成M(OH) n沉淀的pH范围如下:

③常温下,Ksp(CaF2) ═1.46×10-10 Ksp(MgF2) ═7.42×10-11 Ka(HF) ═1.00 ×10-4
回答下列问题:
(1)分析下列图1、图2,氯化铵焙烧锰矿粉的最佳条件是:__________________。

(2)“焙烧”时发生的主要反应的化学方程式为_________________________。
(3)浸出液“净化除杂”过程如下:首先加入MnO2将Fe2+氧化为Fe3+,反应的离子方程式为__________;再调节溶液的pH将Al3+、Fe3+变为沉淀除去;然后加入NH4F将Ca2+、Mg2+沉淀除去,此时溶液pH为6,c(Mg2+)═4.64×10-6 mol·L-1,c(HF)为_________mol·L-1。
(4)碳化结晶时,反应的离子方程式为_____________________________________。
(5)碳化结晶过程中不能用碳酸铵溶液代替碳酸氢铵溶液可能的原因是___________________。
(6)测定碳酸锰产品的纯度。
称取0.5000 g碳酸锰产品于锥形瓶中,加25.00 mL磷酸,加热,碳酸锰全部转化为[Mn(PO4)2]3-,冷却至室温。加水稀释至100 mL,滴加2~3滴指示剂,然后用浓度为0.2000 mol·L-1的硫酸亚铁铵[(NH4)2Fe(SO4)2]标准溶液滴定(反应为:[Mn(PO4)2]3- +Fe2+ ═Mn2+ +Fe3++2PO43-)。重复操作3次,记录数据如下表:
滴定次数 | 0.2000 mol·L-1的硫酸亚铁铵标准溶液读数(mL) | |
滴定前 | 滴定后 | |
1 | 0.10 | 20.20 |
2 | 1.32 | 21.32 |
3 | 1.05 | 20.95 |
则产品的纯度=__________,若滴定终点时发现滴定管尖嘴处产生了气泡,则测得的碳酸锰粗产品的纯度___(填“偏高”“ 偏低”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com