
| A. | 容量瓶在使用前应检奄是否漏水 | |
| B. | 实验室需要950mL 0.1mol•L-1NaC1溶液,配制时应选用1000mL容量瓶 | |
| C. | 若移液前容量瓶内有少量水,会使所配溶液浓度偏低 | |
| D. | 配制一定物质的量浓度的溶液时,两次用到玻璃棒,其作用分别是搅拌和引流 |
分析 A.容量瓶在使用前要检查是否漏水;
B.实验室没有950mL的容量瓶,需选用1000mL的容量瓶;
C.整个溶液的体积是通过容量瓶来控制的,在定容时就要加蒸馏水,所以容量瓶不需要干燥;
D.在配制一定物质量浓度的氯化钠溶液时,玻璃棒在溶解氯化钠固体时的作用是搅拌,在移液时的作用是引流.
解答 解:A.容量瓶在使用前要检查是否漏水,防止在摇匀时渗漏,故A正确;
B.实验室没有950mL的容量瓶,需选用1000mL的容量瓶来配制,使用时取用950mL即可,故B正确;
C.整个溶液的体积是通过容量瓶来控制的,在定容时就要加蒸馏水,所以移液前容量瓶内有少量水,对所配溶液浓度无影响,故C错误;
D.在配制一定物质量浓度的氯化钠溶液时,玻璃棒在溶解氯化钠固体时的作用是搅拌,在移液时的作用是引流,故D正确;
故选C.
点评 本题考查了一定物质的量浓度溶液的配制过程中的注意示项,属于基础型题目,易错点是容量瓶规格的选择,难度不大.


科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 负极反应式为Mg-2e-=Mg2+ | |
| B. | 电池放电时Cl-由正极向负极迁移 | |
| C. | 正极反应式为Ag++e-=Ag | |
| D. | 负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| J | ||||
| R |
 ;
;| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入H2的物质的量 | 加入甲的物质的量 |
| y | 甲的物质的量 | 平衡常数K | 甲的转化率 | 生成物物质的量总和 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2和SO2 | B. | Ca(OH)2和Cu(OH)2 | C. | H2SO4和H3PO4 | D. | ZnSO4和CuSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 开始正反应速率最大 | |
| B. | V正(SO2):V正(O2)=2:1时,反应达到平衡状态 | |
| C. | 达到平衡V逆(SO3)最大 | |
| D. | 开始时V逆(SO3)=0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
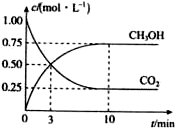 为减小CO2对环境的影响,在倡导“低碳”的同时,还需加强对CO2创新利用的研究.已知:CO2(g)+3H2(g)$\frac{\underline{\;高温\;}}{\;}$CH3OH(g)+H2O(g)△H=-49.0kJ/mol.T1℃时,向体积为1L的恒容密闭容器中充入l mol CO2和3mol H2测得CO2和CH3OH(g)的浓度随时间变化的曲线如图所示,且平衡时体系压强为p1.下列叙述中不正确的是( )
为减小CO2对环境的影响,在倡导“低碳”的同时,还需加强对CO2创新利用的研究.已知:CO2(g)+3H2(g)$\frac{\underline{\;高温\;}}{\;}$CH3OH(g)+H2O(g)△H=-49.0kJ/mol.T1℃时,向体积为1L的恒容密闭容器中充入l mol CO2和3mol H2测得CO2和CH3OH(g)的浓度随时间变化的曲线如图所示,且平衡时体系压强为p1.下列叙述中不正确的是( )| A. | 0~3 min内,v(CO2)正=v(CH3OH)正 | |
| B. | 在T1℃时,若起始时向容器中充人2 moI CO2和6 mol H2,测得平衡时容器内压强为p2,则p2<2p1 | |
| C. | 其他条件不变,若向平衡后的体系中充人1 mol氦气,体系压强增大,平衡将向正反应方向移动 | |
| D. | T2℃时,上述反应平衡常数为4.2,则T2>T1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com