
【题目】甲醇是一种重要的化工原料,有着重要的用途和应用前景。
(1)工业上常用CO和H2合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g) △H
CH3OH(g) △H
①已知:aA(g)+bB(g)=xX(g)+yY(g) △H=x△Hm[X(g)]+y△Hm[Y(g)]-a△Hm[A(g)]-b△Hm[B(g)]。
△Hm[X(g)]表示X(g)的摩尔生成焓,其余类推。25℃101kPa时,CO(g)、H2(g)、CH3OH(g)的摩尔生成焓分别为-110.5kJ·mol-1、0、-201.2kJ·mol-1,则上述反应的△H=_____。
②某温度下,向容积为2L的密闭容器中加入1molCO和2molH2,发生上述反应,CO转化率随时间的变化如图所示:
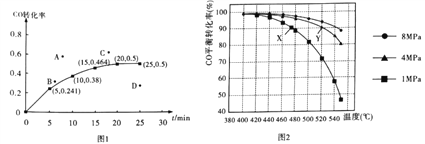
该温度下反应的平衡常数为_______;若起始压强为9MPa,则10min时容器中的压强为_______;若保持其它条件不变,起始时加入2molCO和2molH2,达到平衡,相应的点可能是上图A、B、C、D中的____。
③若只改变反应的一个条件,能使平衡体系中![]() 增大的措施有_______________(答出两点即可)。
增大的措施有_______________(答出两点即可)。
④若投料时CO与H2的物质的量之比恒定,温度、压强对CO平衡转化率的影响如图所示,如图中X点的v(逆)____________Y点的v(正)(填“>”“<”或“=”),理由是_____________。
(2)工业上常用CH3OH来制备HCOOH(甲酸)。已知25℃时,0.1mol·L-1HCOOH溶液的pH为2.3,则甲酸的电离度计算式为______;向0.1mol·L-1HCOOH溶液中加水或加入少量HCOONa晶体时,会引起同样变化的是_______(填编号)。
A.溶液的pH增大 B.HCOOH的电离程度增大
C.溶液的导电能力减弱 D.溶液中c(OH-)减小
【答案】 -90.7 kJ·mol-1 4.0 L2·mol-2 6.72 Mpa B 降温,加压或增加CO的浓度(1分,任答两点) < Y点对应的温度和压强(浓度)都比X点高,温度升高,或压强增大,都会加快反应速率 ![]() ×100% (或10-1.3×100%) A
×100% (或10-1.3×100%) A
【解析】(1)①根据摩尔生成焓定义可知,△H=-201.2kJ·mol-1-(-110.5kJ·mol-1)-0=-90.7 kJ·mol-1。
②由图像可知,平衡时CO的转化率为50%。根据三段式可知,
CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
起始浓度(mol/L) 0.5 1 0
转化浓度(mol/L) 0.25 0.5 0.25
平衡浓度(mol/L) 0.25 0.5 0.25
则该温度下反应的平衡常数为![]() =4.0 L2·mol-2。
=4.0 L2·mol-2。
10min时,CO的转化率为38%。根据三段式可知,
CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
起始物质的量(mol) 1 2 0
转化物质的量(mol) 0.38 0.76 0.38
平衡物质的量(mol) 0.62 1.24 0.38
相同的温度、体积下,压强之比等于物质的量之比,![]() =
=![]() ,解得容器中的压强为6.72 Mpa。
,解得容器中的压强为6.72 Mpa。
若保持其它条件不变,起始时加入2molCO和2molH2,化学反应速率更快,达到平衡所需时间比原平衡的短,且CO的转化率更低,故选A。
③若只改变反应的一个条件,使平衡体系中![]() 增大,可使平衡正向移动,采取的措施有降温,加压或增加CO的浓度等。
增大,可使平衡正向移动,采取的措施有降温,加压或增加CO的浓度等。
④由图可知,图像上各点都为对应温度下的平衡点,即正逆反应速率相等。Y点对应的温度和压强(浓度)都比X点高,温度升高,或压强增大,都会加快反应速率,所以图中X点的v(逆)<Y点的v(正)。
(2)25℃时,0.1mol·L-1HCOOH溶液的pH为2.3,则氢离子浓度为10-2.3 mol·L-1,所以已电离的甲酸浓度为10-2.3 mol·L-1,则甲酸的电离度为![]() ×100%。
×100%。
向0.1mol·L-1HCOOH溶液中加水,甲酸的电离平衡正向移动,电离程度增大,但c(H+)减小,溶液的pH增大,溶液的导电能力减弱,c(OH-)增大;加入少量HCOONa晶体时,平衡逆向移动,电离程度减小,c(H+)减小,溶液的pH增大,溶液的导电能力增强,c(OH-)增大;故选A。


 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是
A. 常温下,5.6g Fe与含0.2mol HNO3的溶液充分作用,最少会失去电子数为0.15NA
B. 3g![]() 所含的电子数为1.8NA
所含的电子数为1.8NA
C. 常温下,1L 0.1mol/L AlCl3溶液中阳离子数目小于0.1NA
D. 15.6g Na2O2 和Na2S的固体混合物中,含有阴离子数目为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(乙二酸)存在于自然界的植物中,其K1=5.4×10-2,K2=5.4×10-5。草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸晶体(H2C2O42H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解。请回答下列问题:
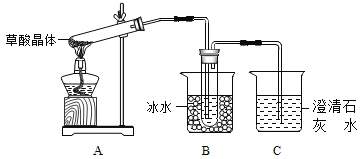
(1)甲组同学按照上图所示装置,通过实验检验草酸晶体的分解产物。装置C中可观察到的现象是_______,由此可知草酸晶体分解的产物中有__________。装置B的主要作用是_____________。
(2)乙组同学认为草酸晶体分解产物中还有CO,为进行验证,选用甲组实验中的装置A、B和下图所示的部分装置(可以重复选用)进行实验。
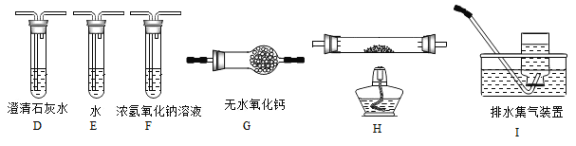
①乙组同学的实验装置中,依次连接的合理顺序为A、B_____________。
装置H反应管中盛有的物质是_________________。
②能证明草酸晶体分解产物中有CO的现象是_________________。
(3)设计实验证明:
①草酸的酸性比碳酸的强_____________。
②草酸为二元酸___________________。
(4)草酸和草酸钠(Na2C2O4)可以在酸性条件下被KMnO4溶液、MnO2氧化,锰元素被还原为+2价。KMnO4溶液和草酸钠溶液在稀硫酸中反应的离子方程式为:________________。
实验室常用固体草酸钠测定KMnO4溶液的浓度。准确称取0.2000g草酸钠,放入锥形瓶中,加入100mL稀硫酸溶解,用配制好的KMnO4溶液滴定,三次重复实验消耗KMnO4溶液的体积分别是16.02mL、16.00 mL、16.01 mL,则KMnO4溶液的物质的量浓度的计算式是:c(KMnO4)=_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,调节2.0×10-3 mol/L氢氟酸水溶液的pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系如图所示。请结合图中信息回答下列问题:
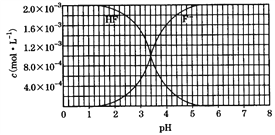
(1)HF电离平衡常数的表达式:Ka=_________。室温下,向HF溶液中滴加NaOH溶液至pH=3.4时,c(F-)∶c(HF) =_______。HF 的电离常数值为_______。
(2)将4.0×10-3mol/L的HF溶液与4.0×10-4mol/LCaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化),通过列式计算说明是否有沉淀产生:
______________________________。[已知Ksp(CaF2)=1.5×10-10 ]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各反应中,乙醇分子断裂C—O键而失去羟基的是
A.乙醇在浓硫酸存在下发生消去反应
B.乙醇与金属钠反应
C.乙醇氧化为乙醛
D.与乙酸反应生成乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。
![]()
![]()
![]()
![]()
![]()
回答下列问题:
(1)为尽量少引入杂质,试剂①应选用NaOH溶液,若选用H2SO4溶液,其后果是_________。
(2)易拉罐溶解过程中主要反应的化学方程式为_______________;滤液A中的某种离子与NH4+,HCO3-均能反应生成沉淀B,该离子与NH4+反应的离子方程式为___________。
(3)Al(OH)3在水中存在两种电离方式,其中:Al(OH)3(aq)![]() AlO2-+H+(aq)+H2O(l) Ka=2.0×10-13(25℃),则25℃时Al(OH)3与NaOH溶液反应的平衡常数K=________________(列出含Kw、Ka的表达式并计算)
AlO2-+H+(aq)+H2O(l) Ka=2.0×10-13(25℃),则25℃时Al(OH)3与NaOH溶液反应的平衡常数K=________________(列出含Kw、Ka的表达式并计算)
(4)明矾与硫磺焙烧时发生反应的化学方程式为:KAl(SO4)2·12H2O+S![]() K2SO4+Al2O3+SO2↑+H2O(未配平),配平后的化学计量数依次为____________;每生成67.2L标准状况下的SO2,转移电子的物质的量为________;焙烧产生的SO2经催化氧化、吸收等过程可制得硫酸,若SO2催化氧化时的转化率为96.0%,则理论上用该法生成硫酸时硫元素的总转化率为__________。
K2SO4+Al2O3+SO2↑+H2O(未配平),配平后的化学计量数依次为____________;每生成67.2L标准状况下的SO2,转移电子的物质的量为________;焙烧产生的SO2经催化氧化、吸收等过程可制得硫酸,若SO2催化氧化时的转化率为96.0%,则理论上用该法生成硫酸时硫元素的总转化率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取ag某物质在氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后固体的质量恰好也增加ag.下列物质中不能满足上述结果的是( )
A. H2 B. CO C. CH4 D. H2和CO的混合气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用铅蓄电池对下图装置进行供电,能模拟植物光合作用,将简单无机物转化为O2和C3H8O,下列说法不正确的是
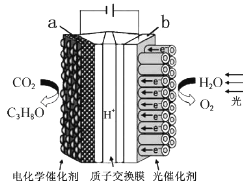
A. 该装置实现了将太阳能、电能转化为化学能
B. b极上每生成0.1molO2,铅蓄电池的负极增重19.2g
C. a极上每生成0.1molC3H8O,有1.8mol电子发生转移
D. 质子交换膜的作用是传导电子、平衡电荷,沟通回路
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com