
| A.电池工作时,MnO2失去电子 |
| B.电池工作时,电子由锌经外电路流向MnO2 |
| C.从反应方程式来看,不使用氢氧化钾,也不影响电流大小 |
| D.电池的正极反应式为2MnO2(s)+H2O(l)+2e-=Mn2O3(s)+2OH-(aq) |
 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源:不详 题型:单选题
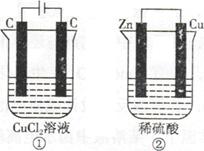
| A.产生气体的体积:①>② |
| B.溶液的pH变化:①减小,②增大 |
| C.电极上生成物质的质量:①=② |
| D.电极反应式:①中阳极2Cl—-2e—=Cl2↑,②中负极2H++2e—=H2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.X电极是负极,电极反应式为CH4-8e-+4CO32-=5CO2+2H2O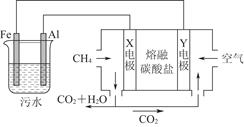 |
| B.铁作阳极,失去电子生成Fe2+ |
| C.工作时熔融盐中的碳酸根移向Y电极 |
| D.污水中存在反应4Fe2++10H2O+O2=4Fe(OH)3↓+8H+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
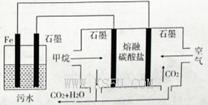
A.铁电极的电极反应式为: |
B.通人空气的石墨电极的电极反应式为 |
| C.若左池石墨电极产生44. 8L(标准状况)气体,则消耗氧气0. 5mol |
| D.为增强污水的导电能力,可向污水中加入适量工业用食盐 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2CO32- + 6H2O,则下列说法正确的是
2CO32- + 6H2O,则下列说法正确的是| A.构成该电池的正极和负极必须是两种活性不同的金属 |
| B.充电时有CH3OH生成的电极为阳极 |
| C.放电时溶液中的OH- 移向正极 |
| D.放电时负极的电极反应为:CH3OH-6e-+8OH- = CO32- + 6H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
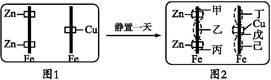
| A.甲区呈现蓝色 | B.乙区呈现红色 |
| C.戊区产生Cu2+离子 | D.丁区产生Fe3+离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Sn2+ (aq)+Pb(s) △H<0,设计成如下图所示的原电池,一段时间后,灵敏电流计读数为零。则下列判断不正确的是( )
Sn2+ (aq)+Pb(s) △H<0,设计成如下图所示的原电池,一段时间后,灵敏电流计读数为零。则下列判断不正确的是( )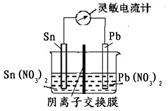
| A.此时化学反应达到平衡状态 |
| B.若此时将Sn电极换成质量较大的Sn 电极后,电流计指针偏转,c(Pb2+)将减小 |
| C.若此时向左池加入少量的Sn(NO3)2固体,电流计指针偏转,Sn电极为正极 |
| D.若此时升高温度,c(Sn2+)将减小,Pb电极为负极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在空气中金属铝表面迅速氧化形成保护层 |
| B.镀锌铁表面有划损时,也能阻止铁被氧化 |
| C.红热的铁丝与冷水接触,表面形成蓝黑色保护层 |
| D.浓硝酸比稀硝酸更能氧化金属铜 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
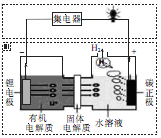
| A.电池工作时,锂离子向正极移动 |
| B.有机电解质可用水溶液代替 |
| C.电池总反应为2Li + 2H2O="2LiOH" + H2↑ |
| D.该装置不仅可提供电能,还可得到清洁的氢气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com