
【题目】1,4-环乙二醇可通过下列路线合成(某些反应的反应物和反应条件未列出):

(1)写出反应④、⑦的化学方程式:
④____________________________________________;
⑦____________________________________________。
(2)①的反应类型是_________,②的反应类型是_________,上述七个反应中属于加成反应的有_________(填反应序号),A中所含有的官能团名称为_________。
(3)反应⑤中可能产生一定量的副产物,其可能的结构简式为__________________。
【答案】 
![]() 取代反应 消去反应 ③⑤⑥ 碳碳双键
取代反应 消去反应 ③⑤⑥ 碳碳双键 
【解析】由合成路线可以知道,反应①为光照条件下的取代反应,反应②为NaOH/醇条件下的消去反应生成A为![]() ,A发生反应③为烯烃与氯气加成生成B为
,A发生反应③为烯烃与氯气加成生成B为 ,B发生反应④得到两个C=C键,则为NaOH/醇条件下的消去反应,反应⑤为溴与环已二烯的1,4加成反应,反应⑥为烯烃与氢气的加成反应,生成C为
,B发生反应④得到两个C=C键,则为NaOH/醇条件下的消去反应,反应⑤为溴与环已二烯的1,4加成反应,反应⑥为烯烃与氢气的加成反应,生成C为![]() ,反应⑦NaOH/水条件下的水解反应生成对环己二醇,据此答题。
,反应⑦NaOH/水条件下的水解反应生成对环己二醇,据此答题。
(1)根据以上分析可知,B为 ,在NaOH醇溶液中加热发生消去反应,反应的方程式为
,在NaOH醇溶液中加热发生消去反应,反应的方程式为 ;根据以上分析可知有机物C为
;根据以上分析可知有机物C为![]() ,在氢氧化钠水溶液中加热发生取代反应,反应的方程式为:
,在氢氧化钠水溶液中加热发生取代反应,反应的方程式为:![]() ;正确答案:
;正确答案: ;
;![]() 。
。
(2)反应①为光照条件下的取代反应;反应②为NaOH/醇条件下的消去反应生成A为![]() ,含有官能团为碳碳双键;反应③为烯烃与氯气加成生成B为
,含有官能团为碳碳双键;反应③为烯烃与氯气加成生成B为 ,B发生反应④得到两个C=C键,则为NaOH/醇条件下的消去反应,反应⑤为溴与环已二烯的1,4加成反应,反应⑥为烯烃与氢气的加成反应,生成C为
,B发生反应④得到两个C=C键,则为NaOH/醇条件下的消去反应,反应⑤为溴与环已二烯的1,4加成反应,反应⑥为烯烃与氢气的加成反应,生成C为![]() ,反应⑦NaOH/水条件下的水解反应生成对环己二醇,综上所述,七个反应中属于加成反应的有③⑤⑥ ;正确答案:取代反应 ;消去反应; ③⑤⑥; 碳碳双键。
,反应⑦NaOH/水条件下的水解反应生成对环己二醇,综上所述,七个反应中属于加成反应的有③⑤⑥ ;正确答案:取代反应 ;消去反应; ③⑤⑥; 碳碳双键。
(3)共轭二烯与溴发生加成反应,如果和溴1:1加成,有1,4加成,结构为![]() ,有1,2加成,结构为
,有1,2加成,结构为![]() ;如果和溴1:2加成,结构为
;如果和溴1:2加成,结构为 ,反应⑤中副产物的结构简式可能为:
,反应⑤中副产物的结构简式可能为: ;正确答案:
;正确答案: 。
。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】化学与人类生活密切相关。回答下列问题:
(1)食品和药品关系人的生存和健康。
①市场上销售的食盐品种很多。下列食盐中,所添加的元素不属于人体必需微量元素的是__________(填序号字母,下同);
a.加钙盐 b.加碘盐 C.加锌盐
②纤维素被称为“第七营养素”。食物中含有的纤维素虽然不能为人体提供能量,但能促进肠道蠕动、吸附排除有害物质。在对有机物的分类中,纤维素属于__________;
a.蛋白质 b.脂肪 c.多糖
③下列药品中,服用后具有退烧效果的是_____________。
a.复方甘草麻黄碱片 b.复方阿司匹林片 c.复方氢氧化铝片
(2)材料是人类生存和发展的物质基础.合理使用材料可以改善我们的生活。
①在原子反应堆中广泛应用的钠钾合金在常温下呈液态.说明合金的熔点比其各成分金属的熔点___(选填“高”或“低”);
②炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会出现红褐色锈斑。我们将这种腐蚀方式称为_________________;
③人工合成的塑料有多种,其中聚丙烯是常见的食品级塑料,写出聚丙烯的结构简式__________。
(3)防治环境污染,改善生态环境已成为全球共识。
①下列物质中,进入大气会形成酸雨的是____________(填序号字母);
a.碳氧化物 b.硫氧化物 c.氮氧化物
②为治理“白色污染”,有人提出把塑料垃圾集中露天焚烧,这种处理方法的弊端是:__________(写出两项即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砹(At)是卤族元素中位于碘后面的元素,下列有关砹的说法不正确的是( )
A.最外层有7个电子B.原子半径比碘大
C.易失去电子D.得到电子能力比碘弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,11.2 LHCl气体中含有的分子数为0.5NA
B. 常温常压下,5.6 g N2和CO混合物中所含有的原子数为0.4NA
C. 将0.2 mol FeCl3水解制成胶体,所得胶体粒子数为0.2NA
D. 50 mL12 mol/L盐酸与足量MnO2共热,转移电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制乙烯时,产生的气体能使溴水褪色,甲、乙同学用下列实验验证。
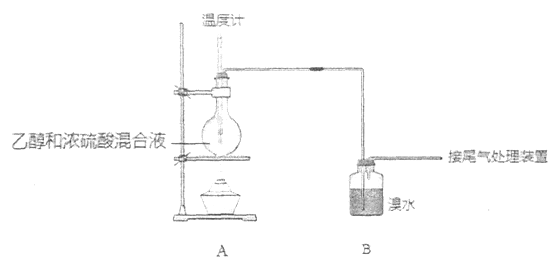
(气密性已检验,部分夹持装置略)。实验操作和现象为:
操作 | 现象 |
点燃酒精灯,加热至170℃ | I:A中烧瓶内液体渐渐变黑 II:B内气泡连续冒出,溶液逐渐褪色 |
…… | |
实验完毕,清洗烧瓶 | III:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(1)烧瓶内产生乙烯的化学方程式是________。
(2)溶液“渐渐变黑”,说明浓硫酸具有________性。
(3)分析使B中溶液褪色的物质,甲认为是C2H4,乙认为不能排除SO2的作用。
①根据甲的观点,使B中溶液褪色反应的化学方程式是________。
②乙根据现象III认为产生了SO2,在B中与SO2反应使溶液褪色的物质是________。
③为证实各自观点,甲、乙重新实验,设计与现象如下:
设计 | 现象 | |
甲 | 在A、B间增加一个装有某种试剂的洗气瓶 | 溴水褪色 |
乙 | 与A连接的装置如下:
| D中溶液由红棕色变为浅红棕色时,E中溶液褪色 |
a. 根据甲的设计,洗气瓶中盛放的试剂是________。
b. 根据乙的设计,C中盛放的试剂是________。
c. 能证明确实是SO2使E中溶液褪色的实验是________。
d. 乙为进一步验证其观点,取少量D中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是________。
(4)上述实验得到的结论是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.2mol有机物和0.4mol O2在密闭容器中燃烧后产物为CO2,CO和H2O(g)。产物经过浓H2SO4后,质量增加10.8g;再通过灼热的CuO,充分反应后,CuO质量减轻3.2g,最后气体再通过碱石灰被完全吸收,质量增加17.6g。
(1)试推断该有机物的分子式________。
(2)若0.2 mol该有机物恰恰将与9.2g金属钠完全反应,试确定该有机物的结构简式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次增大,A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子最外层电子数之和与C原子的最外层电子数相等;D原子有两个电子层,最外层电子数是次外层电子数的3倍。(提示:10电子微粒是指该微粒(包括分子、原子、离子)有10个电子,如H2O、OH-、Na+、Mg2+、CH4、NH4+、NH3等)
(1)试写出它们的元素符号:
A________,B___________,C__________,D___________。
(2)甲、乙、丙、丁是含有以上元素中的一种或几种组成的10电子微粒;
①甲为分子,且能刻蚀玻璃,则甲的化学式为______
②乙为气体,且遇到无色酚酞溶液变成红色,则乙的化学式为_______
③丙为阳离子,丁为阴离子,且丙和丁在加热条件下生成的两种物质也是10电子微粒,请写出该反应方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,浓硫酸既表现出强氧化性又表现出酸性的是( )
A. 2NaCl+H2SO4(浓)![]() Na2SO4+2NaClB. Na2SO3+H2SO4(浓)
Na2SO4+2NaClB. Na2SO3+H2SO4(浓)![]() Na2SO4+SO2↑+H2O
Na2SO4+SO2↑+H2O
C. C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2OD. 2FeO+4H2SO4(浓)
CO2↑+2SO2↑+2H2OD. 2FeO+4H2SO4(浓)![]() Fe2(SO4)3+SO2↑+4H2O
Fe2(SO4)3+SO2↑+4H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com