
 ��
��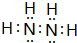
���� A��B��C��D��E���ֶ���������Ԫ���У����ǵ�ԭ��������������A��B��ɵ���̬�������ˮ��Һ�ʼ��ԣ���AΪHԪ�ء�BΪNԪ�أ�A��D������C��ԭ�Ӹ�����Ϊ1��1��2��1�γɵĻ������CΪOԪ�ء�DΪNa��E��C��������������ͬ����EΪSԪ�أ��ݴ˽��
��� �⣺A��B��C��D��E���ֶ���������Ԫ���У����ǵ�ԭ��������������A��B��ɵ���̬�������ˮ��Һ�ʼ��ԣ���AΪHԪ�ء�BΪNԪ�أ�A��D������C��ԭ�Ӹ�����Ϊ1��1��2��1�γɵĻ������CΪOԪ�ء�DΪNa��E��C��������������ͬ����EΪSԪ�أ�
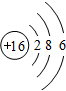
��1��EΪSԪ�أ�ԭ�ӽṹʾ��ͼΪ�� ��
��
�ʴ�Ϊ�� ��
��
��2��A��B�γɺ���18���ӵĻ������ΪN2H4�������ʽΪ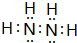 ��
��
�ʴ�Ϊ��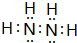 ��
��
��3��D��C��ԭ�Ӹ�����Ϊ1��1�γɻ�������ΪNa2O2����ˮ��Ӧ�����ӷ���ʽ��2Na2O2+2H2O=4Na++4OH-+O2����
�ʴ�Ϊ��2Na2O2+2H2O=4Na++4OH-+O2����
��4�����ڷǽ�����O��N�����⻯���ȶ��ԣ�H2O��NH3��
�ʴ�Ϊ��H2O��NH3��
��5��F��һ����ʷ�ƾá�Ӧ�ù㷺�Ľ���Ԫ�أ�����F����Ͷ�뵽������Һ�У�������dz��ɫ��ҺM����FΪFe��MΪFeCl2��A�� C��ԭ�Ӹ�����Ϊ1��1�γɵĻ������ΪH2O2�������������ǿ�����ԣ���������������Ϊ�����ӣ���Ӧ�����ӷ���ʽ��2Fe2++H2O2+2H+=2Fe3++2H2O��
�ʴ�Ϊ��2Fe2++H2O2+2H+=2Fe3++2H2O��
��6����H2��N2Ϊ�缫��Ӧ���HCl-NH4Cl��ҺΪ�������Һ��������ȼ�ϵ�أ����ڵ����ɸ������������������ƶ����ʷŵ�ʱ��Һ��H+�������������������������
�ʴ�Ϊ������
���� ������Ԫ���ƶ�Ϊ���壬����λ�ýṹ���ʹ�ϵ������ʽ��ԭ�ӽṹʾ��ͼ��Ԫ�������ɡ�Ԫ�ػ��������ʡ�ԭ��صȣ���Ŀ�Ƚ��ۺϣ��ؼ��Ǹ�����������ƶ�Ԫ�أ���Ҫѧ���߱���ʵ�Ļ�������Ŀ�Ѷ��еȣ�


 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���к�ǿ��������� | B�� | ��һ��ʮ���ȶ��Ļ����� | ||
| C�� | ����ǿ���忹������ | D�� | ���г�����������ɱ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | CuO+2HCl�TCuCl2+H2O | B�� | 2Na2O2+2H2O�T4NaOH+O2�� | ||
| C�� | Zn+CuSO4�TZnSO4+Cu | D�� | Ca��OH��2+CO2�TCaCO3��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��� | ʵ������ | �Լ� | ����ͽ��� |
| �� | ����K2CO3��Na2SO3 | ���ᡢ�����ʯ��ˮ | ������ɫ��ζ���壬��ʹ�����ʯ��ˮ����ǵ���K2CO3 |
| �� | ����NO2��Br2���� | ʪ��ĵ���KI��ֽ | ��ֽ����ɫ����Br2���� |
| �� | ��ȥ�Ȼ�����Һ�е��Ȼ������� | ̼��� | ������Һ��pHΪ3.7���ٹ��� |
| A�� | �٢ڢ� | B�� | �� | C�� | �٢� | D�� | �٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
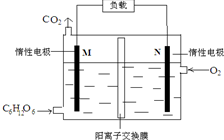 һ��������ˮ����װ��ģ��ϸ���������IJ������̣��ɽ������л���ˮ�Ļ�ѧ��ֱ��ת��Ϊ���ܣ�����˵���в���ȷ���ǣ�������
һ��������ˮ����װ��ģ��ϸ���������IJ������̣��ɽ������л���ˮ�Ļ�ѧ��ֱ��ת��Ϊ���ܣ�����˵���в���ȷ���ǣ�������| A�� | �������C6H12O6��ȫȼ�շ��ȱȽϣ���װ�÷���Ч�ʸ� | |
| B�� | ���øõ�ص����������������N�������ĵ缫���������� | |
| C�� | ��������M�����ء�N���������Һ��M | |
| D�� | ��N������5.6L������£�����ʱ�������NA��H+ͨ�������ӽ���Ĥ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢۢ� | B�� | �٢ڢۢ� | C�� | �ڢۢܢ� | D�� | ȫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ȷ�Ӧ�������¶ȣ�v������v����С | |
| B�� | �����κλ�ѧ��Ӧ��˵����Ӧ����Խ��Ӧ���ת����Խ�� | |
| C�� | ���������ķ�Ӧ�ﵽƽ�������ѹǿ��ƽ����ܲ��ƶ� | |
| D�� | ѡ���ʵ��Ĵ����������˶��ӿ죬��������ײƵ�ʣ��ʷ�Ӧ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��ѧʽ | CH3COOH | HClO | H2CO3 |
| Ka | Ka=1.8��10-5 | Ka=3.0��10-8 | Ka1=4.1��10-7 Ka2=5.6��10-11 |
| A�� | ��ͬpH����������Һ�����ʵ���Ũ���ɴ�С��˳��Ϊ��c��HClO����c��CH3COOH����c��H2CO3�� | |
| B�� | ����ͬ���ʵ���Ũ�ȵ�Na2CO3��NaClO��NaHCO3��CH3COONa���������м�ˮϡ�ͣ�ˮ��̶Ⱦ������Ծ���ǿ | |
| C�� | �����ʵ���Ũ�ȵ�NaClO��NaHCO3 �����Һ�У�c��Na+��=c��HClO��+c��ClO-��+c��HCO3-��+c��CO32-��+c��H2CO3�� | |
| D�� | �����������Һ��ͨ������������̼��������ӷ���ʽΪ��2ClO-+CO2+H2O�TCO32-+2HClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
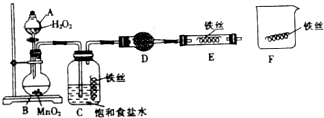
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com