
| A. | 煤的干馏和煤的液化均是物理变化 | |
| B. | 船体镀锌或锡均可保护船体,镀层破损后将立即失去保护作用 | |
| C. | 由于共价键具有方向性,共价化合物在形成晶体时均采取“紧密堆积” | |
| D. | 反应NH4Cl (s)═NH3(g)+HCl(g)室温下不能自发进行,则该反应的△H>0 |
分析 A.煤的干馏和煤的液化都是化学变化;
B.原电池的负极是容易有被氧化的电极,易被腐蚀;
C.共价化合物原子晶体不能紧密堆积,不遵循“紧密堆积”原理;
D.当△G=△H-T•△S>0时,反应不能自发进行.
解答 解:A.煤的干馏是指将煤隔绝空气加强热使之分解的过程,煤液化生成甲醇,属于化学变化,故A错误;
B.锌活泼性强于铁,锡活泼性弱于铁,镀锌铁破损后仍然能够保护铁,镀锡铁破损后加速铁的腐蚀,故B错误;
C.原子晶体是原子以具有方向性和饱和性的共价键结合形成的,不能紧密堆积,不遵循“紧密堆积”原理,故C错误;
D.化学反应能否自发进行,取决于焓变和熵变的综合判据,当△G=△H-T•△S<0时,反应能自发进行,当△H<0,△S>0时,△G=△H-T•△S<0,在室温一定能自发进行,而△H>0,△S<0时不能自发进行,该反应的△S>0,反应:NH4Cl (s)═NH3(g)+HCl(g)在室温下不能自发进行,则室温下△G=△H-T•△S>0,说明△H>0,故D正确;
故选D.
点评 本题考查煤的综合利用、金属的腐蚀防护、晶体的堆积方式、反应的方向等知识,内容较为综合,难度不大,注意基础知识的掌握.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
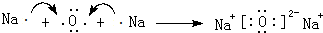 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 化学键 | C-C | C-H | C-O | Si-Si | Si-H | Si-O |
| 键能/(kJ•mol-1 | 356 | 413 | 336 | 226 | 318 | 452 |
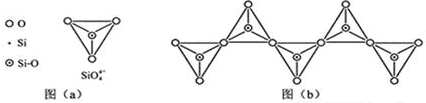
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 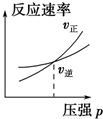 | B. | 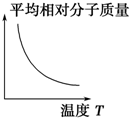 | C. | 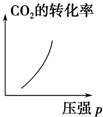 | D. | 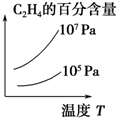 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
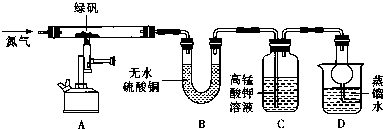
| 装置 | 现象 | 结论 |
| A | 固体呈红棕色,将其放入足量稀盐酸,固体全部溶解,得到黄色溶液 | |
| B | 无水硫酸铜变蓝 | |
| C | 高锰酸钾溶液褪色 |
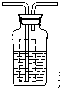 瓶内为0.5mol/L的BaC12溶液,有白色沉淀生成说明分解产物SO3
瓶内为0.5mol/L的BaC12溶液,有白色沉淀生成说明分解产物SO3查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com