
| A. | 氯气和水反应:Cl2+H2O?H++Cl-+HClO | |
| B. | 铁与稀盐酸反应:Fe+2H+═Fe2++H2↑ | |
| C. | 碳酸氢铵溶液与足量澄清石灰水反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| D. | 少量二氧化硫气体通入FeCl3溶液中:2Fe3++SO2+2H2O═2Fe2++4H++SO42- |
分析 A.氯气与水反应生成氯化氢和次氯酸;
B.铁与稀盐酸反应生成氯化亚铁和氢气;
C.澄清石灰水足量,铵根离子也参与反应;
D.铁离子将二氧化硫氧化成硫酸.
解答 解:A.氯气和水反应生成HCl和HClO,反应的离子方程式为:Cl2+H2O?H++Cl-+HClO,故A正确;
B.Fe与稀盐酸反应生成氯化亚铁和H2,反应的离子方程式为:Fe+2H+═Fe2++H2↑,故B正确;
C.碳酸氢铵溶液与足量澄清石灰水反应,漏掉了铵根离子与氢氧根离子的反应,正确的离子方程式为:NH4+++HCO3-+Ca2++2OH-═CaCO3↓+H2O+NH3•H2O,故C错误;
D.少量二氧化硫气体通入FeCl3溶液中,二者发生氧化还原反应,反应的离子方程式为:2Fe3++SO2+2H2O═2Fe2++4H++SO42-,故D正确;
故选C.
点评 本题考查了离子方程式的判断,题目难度不大,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高纯度的硅单质广泛用于制作光导纤维 | |
| B. | 汽车尾气中氮氧化物的产生主要是由于汽油中含有氮元素 | |
| C. | 用蘸有浓氨水的棉棒检验输送氯气的管道是否漏气 | |
| D. | 埃博拉病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  如图,NaCl晶体只有在熔融状态下离子键被完全破坏,才能形成自由移动的离子 | |
| B. | 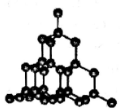 如图,金刚石中存在的化学键只有共价键,不能导电 | |
| C. | 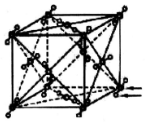 如图,干冰中的化学键只需吸收很少的热量就可以破坏,所以干冰容易升华 | |
| D. | 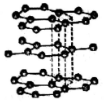 如图,石墨中碳原子的最外层电子都参与了共价键的形成,故熔点很高、硬度很大 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
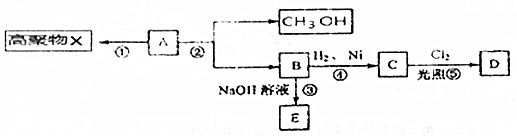
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验现象 | 实验结论 |
| A | 将铝片分别投入浓、稀硝酸中,前者无明显现象,后者反应剧烈 | 稀硝酸的氧化性比浓硝酸的强 |
| B | 滴有酚酞的Na2CO3溶液中加入BaCl2溶液,红色变浅 | Na2CO3溶液中存在水解平衡 |
| C | 某溶液中滴加过量氨水产生白色沉淀且不溶解 | 该溶液中一定含有Mg2+ |
| D | 溴水中通入SO2,溴水褪色 | SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
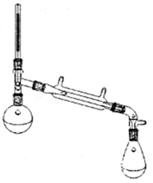 环乙烯是一种重要的化工原料,实验室常用下列反应制备环乙烯:
环乙烯是一种重要的化工原料,实验室常用下列反应制备环乙烯: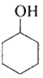 $→_{△}^{H_{2}SO_{4}}$
$→_{△}^{H_{2}SO_{4}}$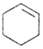 +H2O
+H2O| 物质 | 沸点(℃) | 密度(g•cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)* | 0.9624 | 能溶于水 |
| 环己烯 | 83(70.8)* | 0.8085 | 不溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不慎将酸液溅到眼中,应立即用大量水冲洗,边洗边眨眼睛 | |
| B. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| C. | 洒在桌面上的酒精燃烧,立即用湿抹布盖灭 | |
| D. | 进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com