
 ĪŖĢ½¾æH2O2”¢SO2”¢Br2Ńõ»ÆŠŌĒæČõ£¬Ä³Š”×éĶ¬Ń§Éč¼ĘČēĻĀŹµŃé£Ø¼Š³Ö¼°Ī²Ęų“¦Ąķ×°ÖĆŅŃĀŌČ„£¬ĘųĆÜŠŌŅŃ¼ģŃ飩£®
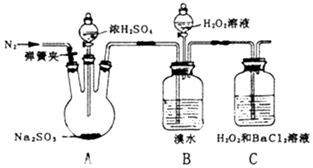
ĪŖĢ½¾æH2O2”¢SO2”¢Br2Ńõ»ÆŠŌĒæČõ£¬Ä³Š”×éĶ¬Ń§Éč¼ĘČēĻĀŹµŃé£Ø¼Š³Ö¼°Ī²Ęų“¦Ąķ×°ÖĆŅŃĀŌČ„£¬ĘųĆÜŠŌŅŃ¼ģŃ飩£®| ŹµŃé²Ł×÷ | ŹµŃéĻÖĻó |
| i£®“ņæŖAÖŠ·ÖŅŗĀ©¶·»īČū£¬µĪ¼ÓÅØĮņĖį | AÖŠÓŠĘųÅŻ²śÉś£¬BÖŠŗģ×ŲÉ«äåĖ®ĶŹÉ«£¬CÖŠÓŠ°×É«³Įµķ |
| ii£®Č”CÖŠ³Įµķ¼ÓČėŃĪĖį | CÖŠ°×É«³Įµķ²»Čܽā |
| iii£®“ņæŖBÖŠ·ÖŅŗĀ©¶·»īČū£¬ÖšµĪµĪ¼ÓH2O2 | æŖŹ¼Ź±ŃÕÉ«ĪŽĆ÷ĻŌ±ä»Æ£¬¼ĢŠųµĪ¼ÓH2O2ČÜŅŗ£¬Ņ»¶ĪŹ±¼äŗ󣬻ģŗĻŅŗÖš½„±ä³Éŗģ×ŲÉ« |
·ÖĪö £Ø1£©ŌŚAÖŠÅØĮņĖįÓėNa2SO3·¢Éśø“·Ö½ā·“Ó¦²śÉśSO2ĘųĢ壬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒNa2SO3£Ø¹Ģ£©+H2SO4£ØÅØ£©=Na2SO4+SO2”ü+H2O£»
£Ø2£©¢ŁÓÉÓŚŌŚ×°ÖĆÖŠŗ¬ÓŠæÕĘų£¬æÕĘųÖŠµÄŃõĘųŗĶSO2ŌŚČÜŅŗÖŠŅ²»į·¢Éś·“Ó¦½«ĘäŃõ»Æ£¬ĖłŅŌŅŅĶ¬Ń§ČĻĪŖ²»ÄÜµĆ³ö“Ė½įĀŪ£¬ČĻĪŖŌŚµĪ¼ÓÅØĮņĖįÖ®Ē°Ó¦Ōö¼ÓŅ»²½²Ł×÷£¬ĻČÅž”æÕĘų£»
¢ŚÓÉÓŚäåµ„ÖŹÓŠ»Ó·¢ŠŌ£¬äåµ„ÖŹŅ²æÉŅŌ½«SO2Ńõ»Æ²śÉśĶ¬ŃłµÄŹµŃéĻÖĻó£¬ĖłŅŌ±ūĶ¬Ń§ČĻĪŖ»¹Ó¦øĆŌŚBŗĶCÖ®¼äŌö¼ÓĻ“ĘųĘæDĄ“³żČ„»Ó·¢µÄäåÕōĘų£¬³£¼ūµÄ³żäåæÉŅŌÓĆCCl4»ņ±½»ņ±„ŗĶNaHSO3ČÜŅŗ£»
£Ø3£©ÓÉÓŚH2SO3²»ĪČ¶Ø£¬ŹÜČČČŻŅ×·Ö½ā²śÉśÓŠĘư׊ŌµÄSO2£¬ĖłŅŌĪŖŃéÖ¤¹Ūµć2£¬Ó¦½ųŠŠµÄŹµŃé²Ł×÷¼°ĻÖĻóŹĒȔɣĮæµĪ¼ÓH2O2ČÜŅŗĒ°µÄBÖŠČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČČ£¬½«ĘųĢåĶØČėĘ·ŗģČÜŅŗÖŠ£¬Ę·ŗģČÜŅŗĶŹÉ«£»
£Ø4£©ĪļÖŹŌŚ·¢ÉśŃõ»Æ»¹Ō·“Ó¦ÖŠŃõ»ÆŠŌĒæµÄæÉŅŌ°ŃŃõ»ÆŠŌČõµÄÖĘČ”³öĄ“£¬ĖłŅŌĶعżÉĻŹöČ«²æŹµŃ飬µĆ³ö½įĀŪ£ŗH2O2”¢SO2”¢Br2Ńõ»ÆŠŌÓÉĒæµ½ČõµÄĖ³ŠņŹĒH2O2£¾Br2£¾SO2£®
½ā“š ½ā£ŗ£Ø1£©ŌŚAÖŠÅØĮņĖįÓėNa2SO3·¢Éśø“·Ö½ā·“Ó¦²śÉśSO2ĘųĢ壬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒNa2SO3£Ø¹Ģ£©+H2SO4£ØÅØ£©=Na2SO4+SO2”ü+H2O£¬
¹Ź“š°øĪŖ£ŗNa2SO3£Ø¹Ģ£©+H2SO4£ØÅØ£©=Na2SO4+SO2”ü+H2O£»
£Ø2£©¢ŁÓÉÓŚŌŚ×°ÖĆÖŠŗ¬ÓŠæÕĘų£¬æÕĘųÖŠµÄŃõĘųŗĶSO2ŌŚČÜŅŗÖŠŅ²»į·¢Éś·“Ó¦½«ĘäŃõ»Æ£¬ĖłŅŌŅŅĶ¬Ń§ČĻĪŖ²»ÄÜµĆ³ö“Ė½įĀŪ£¬ČĻĪŖŌŚµĪ¼ÓÅØĮņĖįÖ®Ē°Ó¦Ōö¼ÓŅ»²½²Ł×÷£¬øĆ²Ł×÷ŹĒ“ņæŖµÆ»É¼Š£¬ĶØČėN2£¬“żÅž»×°ÖĆÄŚæÕĘųŗ󣬹Ų±ÕµÆ»É¼Š£¬
¹Ź“š°øĪŖ£ŗ“ņæŖµÆ»É¼Š£¬ĶØČėN2£¬“żÅž»×°ÖĆÄŚæÕĘųŗ󣬹Ų±ÕµÆ»É¼Š£»
¢ŚÓÉÓŚäåµ„ÖŹÓŠ»Ó·¢ŠŌ£¬äåµ„ÖŹŅ²æÉŅŌ½«SO2Ńõ»Æ²śÉśĶ¬ŃłµÄŹµŃéĻÖĻó£¬ĖłŅŌ±ūĶ¬Ń§ČĻĪŖ»¹Ó¦øĆŌŚBŗĶCÖ®¼äŌö¼ÓĻ“ĘųĘæDĄ“³żČ„»Ó·¢µÄäåÕōĘų£¬DÖŠŹ¢·ÅµÄŹŌ¼ĮŹĒCCl4»ņ±½»ņ±„ŗĶNaHSO3ČÜŅŗ£¬
¹Ź“š°øĪŖ£ŗCCl4»ņ±½»ņ±„ŗĶNaHSO3ČÜŅŗ£»
£Ø3£©ÓÉÓŚH2SO3²»ĪČ¶Ø£¬ŹÜČČČŻŅ×·Ö½ā²śÉśÓŠĘư׊ŌµÄSO2£¬ĖłŅŌĪŖŃéÖ¤¹Ūµć2£¬Ó¦½ųŠŠµÄŹµŃé²Ł×÷¼°ĻÖĻóŹĒȔɣĮæµĪ¼ÓH2O2ČÜŅŗĒ°µÄBÖŠČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČČ£¬½«ĘųĢåĶØČėĘ·ŗģČÜŅŗÖŠ£¬Ę·ŗģČÜŅŗĶŹÉ«£¬
¹Ź“š°øĪŖ£ŗȔɣĮæµĪ¼ÓH2O2ČÜŅŗĒ°µÄBÖŠČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČČ£¬½«ĘųĢåĶØČėĘ·ŗģČÜŅŗÖŠ£¬Ę·ŗģČÜŅŗĶŹÉ«£»
£Ø4£©ĪļÖŹŌŚ·¢ÉśŃõ»Æ»¹Ō·“Ó¦ÖŠŃõ»ÆŠŌĒæµÄæÉŅŌ°ŃŃõ»ÆŠŌČõµÄÖĘČ”³öĄ“£¬ĖłŅŌĶعżÉĻŹöČ«²æŹµŃ飬µĆ³ö½įĀŪ£ŗH2O2”¢SO2”¢Br2Ńõ»ÆŠŌÓÉĒæµ½ČõµÄĖ³ŠņŹĒH2O2£¾Br2£¾SO2£¬¹Ź“š°øĪŖ£ŗH2O2£¾Br2£¾SO2£®
µćĘĄ ±¾Ģāæ¼²éĮĖSO2ĘųĢåµÄŹµŃéŹŅÖĘČ”·½·Ø”¢ĪļÖŹŃõ»ÆŠŌĒæČõ±Č½ĻµÄŃéÖ¤”¢·½³ĢŹ½µÄŹéŠ“µČ£¬ÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 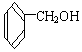 | B£® | 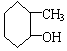 | C£® | 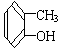 | D£® | 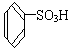 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČ»ÆĀĮ | B£® | Ģ¼ĖįĒāÄĘ | C£® | ĮņĖįĆ¾ | D£® | øßĆĢĖį¼Ų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | æĻ¶ØÓŠµē×ӵƏ§ | |
| B£® | æĻ¶ØŹĒÓŠ¹ŲŃõŌŖĖŲµÄ·“Ó¦ | |
| C£® | æĻ¶ØÓŠ»ÆŗĻ¼ŪµÄ±ä»Æ | |
| D£® | Ńõ»Æ¼ĮµĆµ½µē×Ó×ÜŹżÓė»¹Ō¼ĮŹ§Č„µē×Ó×ÜŹżĻąµČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģ¼ŹĒ·Ē½šŹōŌŖĖŲ£¬ĖłŅŌĢ¼µ„ÖŹ¶¼ŹĒ¾ųŌµĢå | |
| B£® | ÕąŅ²“ęŌŚĘųĢ¬Ēā»ÆĪļ | |
| C£® | ¹¤ŅµÉĻ¹č³£ÓĆĄ“ÖĘČ”¶žŃõ»Æ¹č | |
| D£® | ÕąµÄ·Ē½šŹōŠŌ±Č½šŹōŠŌĒæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļ”ĮņĖįÓėBa£ØOH£©2ČÜŅŗ·“Ӧɜ³É1 molĖ® | |
| B£® | Ļ”ŃĪĖįÓė°±Ė®·“Ӧɜ³É1 mol H2O | |
| C£® | 1 molĻ”H2SO4Óė×ćĮæNaOHČÜŅŗ·“Ó¦ | |
| D£® | Ļ”ŃĪĖįÓėĻ”Ba£ØOH£©2ČÜŅŗ·“Ӧɜ³É1 molĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬2.24 LŅŅ“¼ÖŠŗ¬ÓŠµÄC-H¼üŹżÄæĪŖ0.5NA | |
| B£® | ±ź×¼×“æöĻĀ£¬2.24 L NOŗĶ2.24 L O2»ģŗĻŗóĘųĢå·Ö×ÓŹżĪŖ0.15NA | |
| C£® | Ķس£×“æöĻĀ£¬3.36 LĀČĘųÓė2.7 gĀĮ³ä·Ö·“Ó¦×ŖŅʵĵē×ÓŹżµČÓŚ0.3NA | |
| D£® | ÓÉ1 mol CH3COONaŗĶÉŁĮæCH3COOHŠĪ³ÉµÄÖŠŠŌČÜŅŗÖŠ£¬CH3COO-ŹżÄæĪŖNAøö |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com