
【题目】下列变化不属于化学变化的是 ( )
A.分馏 B.干馏 C.裂化 D.裂解
 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:
【题目】原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置.
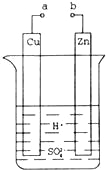
(1)a和b不连接时,烧杯中发生反应的离子方程式是
(2)a和b用导线连接,Cu极为原电池 极(填“正”或“负”),电极反应式是;Zn极发生 (填“氧化”或“还原”)反应,溶液中H+移向 (填“Cu”或“Zn”)极.
(3)a和b用导线连接,若Zn片质量减轻了6.5g,则另一极上理论上产生气体 L(标况下).
(4)有同学向把Ba(OH)28H2O晶体与NH4Cl晶体的反应设计成原电池,你认为是否可行? (填“是”或“否”),理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质对应的用途不正确的是( )
A | B | C | D | |
物质 | Fe2O3 | NH3 | Si | Na2O |
用途 | 作红色涂料 | 制硝酸 | 作半导体材料 | 作供氧剂 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气、铝、铁都是重要的还原剂。已知下列反应的热化学方程式,下列关于反应的焓变判断正确的是( )
2H2(g)+O2(g)=2H2O(g) △H1
3H2 (g) +Fe2O3 (s)=2Fe (s)+3 H2O(g) △H2
2Fe (s)+ 3/2 O2 (g)= Fe2O3 (s) △H3
2Al (s)+ 3/2 O2 (g)= Al2O3 (s) △H4
2Al (s)+ Fe2O3 (s)= Al2O3 (s)+ 2Fe (s) △H5
A.△H1<0 △H3>0 B.△H5<0 △H4<△H3
C.△H1=△H2+△H3 D.△H3=△H4+△H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列各小题中的问题,请用“>”“<”或“=”填空。
(1)质量相同的下列各组物质,所含“物质的量”关系是:
①CO________CO2;
②H2SO4________H3PO4。
(2)相同物质的量的下列各组物质,比较其质量的大小:
①HCl________HF;
②HNO3________H3PO4;
③Mg________Al;
④Na+________Al3+。
(3)比较分子数目多少:
①9 g H2O________11 g CO2;
②1 g H2________1 g O2。
(4)比较下列物质中氢原子数目多少:
①4.9 g H2SO4________5.4 g H2O;
②1.6 g CH4________0.4 g H2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中能大量共存的是( )
A.K + 、SiO32-、OH - 、Na +
B.Na + 、H + 、CO32-、SO42-
C.K + 、H + 、SiO32-、Cl -
D.OH - 、Na + 、HCO3-、Cl –
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大,W与Y最外层电子数之和为X最外层电子数的2倍,Z最外层电子数等于最内层电子数,X、Y、Z简单离子的电子层结构相同,W的单质是空气中体积分数最大的气体.下列说法正确的是( )
A. 元素非金属性由强到弱的顺序:Y、X、W
B. W的简单气态氢化物比Y的简单气态氢化物稳定
C. 原子半径由大到小的顺序:Z、Y、X、W
D. WX与ZX中的化学键类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
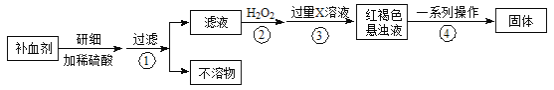
请回答下列问题:
(1)补血剂存放时间较长会氧化变质,对滤液中铁元素的存在形式提出如下假设:
假设1:只有Fe2+
假设2:只有Fe3+
假设3: 。
(2)如何证明步骤①滤液中含有Fe2+ 。
(3)步骤④中一系列处理的操作步骤: 、洗涤、灼烧、 、称量。
(4)该小组有些同学认为可用酸化的KMnO4溶液滴定进行Fe2+含量的测定。
①用离子方程式表示该滴定原理:____________________
②实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯、量筒、药匙、胶头滴管外,还需 。
重复滴定三次,消耗1.00 mol/L KMnO4标准溶液体积分别为19.98 mL、20.00 mL、20.02mL,3次实验所用Fe2+溶液的体积为20.00 mL。请根据以上数据,再设计合理数据,完成下列实验过程的记录表格。(必须填满)
实验编号 | Fe2+溶液的 体积/mL | |||
1 | 20.00 | |||
2 | 20.00 | |||
3 | 20.00 |
③如何判断达到滴定终点:____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com