
| A. | 加压 | B. | 加CuCl2固体 | C. | 加NaCl溶液 | D. | 加醋酸钠固体 |
分析 常见影响反应速率的因素有浓度、温度、压强、催化剂以及固体表面积等,影响硫酸和镁反应的速率的因素有浓度、温度和固体的表面积大小,加快反应速率,应使浓度增大、温度升高或增大固体表面积,不影响生成氢气的总量,则硫酸的物质的量应不变,以此解答.
解答 解:A.为固体和溶液的反应,增大压强,反应速率不变,故A不选;
B.加入氯化铜,镁置换出铜,形成原电池反应,反应速率增大,且不影响生成氢气的总量,故B选;
C.加入氯化钠溶液,浓度减小,反应速率减小,故C不选;
D.加入醋酸钠固体,生成醋酸,氢离子浓度减小,反应速率减小,故D不选.
故选B.
点评 本题考查化学反应速率的影响因素,为高频考点,侧重于学生的分析能力和基础知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大,


科目:高中化学 来源: 题型:解答题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| CO2体积(mL) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | ①中Cu2S、Cu2O只作还原剂 | |
| B. | ①中每生成11.2 L气体(标准状况)转移3 mol原子 | |
| C. | 由反应②可知,在相同条件下的氧化性强弱顺序为:Zn2+>Mn2+>H+ | |
| D. | ②中阳极的电极反应式为:Mn2++2H2O-2e-═MnO2+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
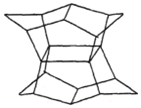 1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子.如图的多环有机分子,因其形状像东方塔式庙宇,所以该分子也就称为pagodane(庙宇烷),有关该分子的说法不正确的是( )
1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子.如图的多环有机分子,因其形状像东方塔式庙宇,所以该分子也就称为pagodane(庙宇烷),有关该分子的说法不正确的是( )| A. | 分子式为C20H20 | B. | 一氯代物的同分异构体只有两种 | ||
| C. | 分子中含有4个亚甲基(-CH2-) | D. | 分子中含有12个五元碳环 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
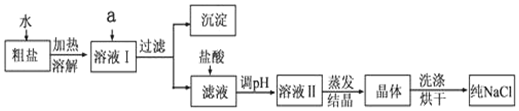
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
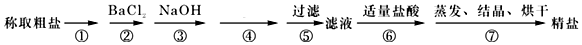
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔质量就是物质的相对分子质量 | B. | 摩尔质量就1mol物质所具有的质量 | ||
| C. | HNO3的摩尔质量是63g | D. | 硫酸和磷酸的摩尔质量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -332 | B. | +260 | C. | +350 | D. | +130 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 科学家合成了具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧热极高.Al2H6球棍模型如图.下列有关说法不正确的是( )
科学家合成了具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧热极高.Al2H6球棍模型如图.下列有关说法不正确的是( )| A. | Al2H6中铝的杂化方式为sp3杂化 | |
| B. | 氢铝化合物可能成为未来的储氢材料和火箭燃料 | |
| C. | Al2H6中含有离子键和极性共价键 | |
| D. | Al2H6在空气中完全燃烧,产物为三氧化二铝和水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com