
| A. | Na2CO3→NaOH | B. | BaCl2→Ba(OH)2 | C. | FeCl3→Fe(OH)3 | D. | CaCO3→CaCl2 |
分析 A.碳酸钠与氢氧化钙反应生成碳酸钙和NaOH;
B.氯化钡不能一步转化为氢氧化钡;
C.氯化铁与碱反应生成氢氧化铁;
D.碳酸钙与盐酸反应生成氯化钙.
解答 解:A.Na2CO3$\stackrel{Ca(OH)_{2}}{→}$NaOH可一步转化,故A不选;
B.BaCl2→Ba(OH)2不能一步转化实现,故B选;
C.FeCl3$\stackrel{NaOH/氨水等}{→}$Fe(OH)3可一步转化,故C不选;
D.CaCO3$\stackrel{HCl}{→}$CaCl2可一步转化,故D不选;
故选B.
点评 本题考查物质的性质及相互转化,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的综合应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
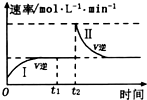 在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)?2C(g)△H<0; t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程(I、Ⅱ)如图所示.下列说法中,一定不正确的是( )
在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)?2C(g)△H<0; t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程(I、Ⅱ)如图所示.下列说法中,一定不正确的是( )| A. | 0~t1时,V正>V逆 | |
| B. | I、Ⅱ两过程分别达到平衡时,A的体积分数Ⅰ>Ⅱ | |
| C. | t2时刻改变的条件可能是向密闭容器中加C物质 | |
| D. | Ⅰ、Ⅱ两过程达到平衡时,平衡常数Ⅰ=Ⅱ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸与氢氧化钡在溶液中反应:Ba2++SO42-═BaSO4↓ | |
| B. | 少量金属钠投入到CuSO4溶液中:2Na+Cu2+═2Na++Cu↓ | |
| C. | BaCO3与盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| D. | 用Cl2将苦卤中的Br-氧化:Cl2+2Br-═2Cl-+Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2是还原产物,且还原剂与氧化剂物质的量之比是2:3 | |
| B. | N2是氧化产物,且还原剂与氧化剂物质的量之比是2:3 | |
| C. | 每转移6mol电子就生成22.4LN2 | |
| D. | NH4Cl是氧化产物,且还原剂与氧化剂物质的量之比是2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 弱电解质在溶液中部分电离,存在电离平衡 | |
| B. | 同一弱电解质的溶液,当温度或浓度不同时,其导电能力也不相同 | |
| C. | 电离常数(K)越小,表示弱电解质电离能力越弱 | |
| D. | 不同浓度的同一弱电解质,其电离常数(K)不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A原子:1s22s22p63s23p63d10 | B. | B2-:1s22s22p6 | ||
| C. | C2+:1s22s22p6 | D. | D原子:1s22s22p6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
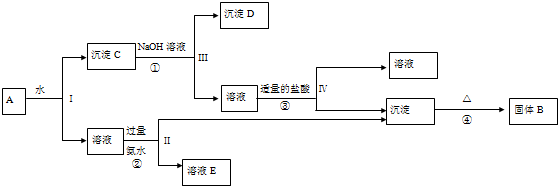
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,
一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
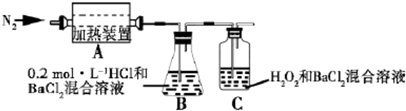
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com