
【题目】过量锌粉与一定量稀盐酸反应,为了减慢反应速率,但又不影响生成的氢气总量,可采取的措施是
A. 升高温度 B. 加入浓度较大的盐酸 C. 加入少量CuSO4 D. 加入适量的水
科目:高中化学 来源: 题型:
【题目】将V1 mL 1.00 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。下列叙述正确的是( )

A. 做该实验时环境温度为22℃
B. NaOH溶液的浓度约为1.00 mol/L
C. 该实验表明有水生成的反应都是放热反应
D. 该实验表明化学能可以转化为热能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M、N两种元素的原子,当它们每个原子获得两个电子形成稀有气体元素原子的电子层结构时,放出的能量M大于N,由此可知( )
①M的氧化性弱于N
②M的氧化性强于N
③N2-的还原性弱于M2-
④N2-的还原性强于M2-
A.①④B.②④C.①②D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式错误的是 ( )
A. Ba(OH)2=Ba2++2OH-
B. NaHSO4(熔融)=Na++H++SO42-
C. MgCl2=Mg2++2Cl-
D. H2SO4=2H++SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向FeBr2、FeI2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示,下列有关说法中不正确的是
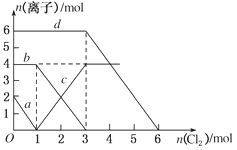
A.d曲线代表溶液中Br-变化情况
B.原溶液中FeI2的物质的量为2 mol
C.原溶液中n(Fe2+):n(Br-)=2:3
D.当通入2 mol Cl2时,溶液中离子反应为2Fe2++2I-+2Cl2===2Fe3++I2+4Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。
制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2。
用现代分析仪器测定TiO2粒子的大小;用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
(1)TiCl4水解生成TiO2·xH2O的化学方程式为:____________________________。
(2)检验TiO2·xH2O中Cl-是否被除净的方法是:____________________________。
(3)可用于测定TiO2粒子大小的方法是____________________(填字母代号)。
a.核磁共振法 b.红外光谱法 c.质谱法 d.透射电子显微镜法
(4)配制NH4Fe(SO4)2标准溶液时,使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要下图中的_________(填字母代号)。
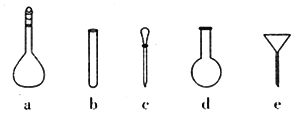
(5)滴定时,称取TiO2(摩尔质量为Mg·mol-1)试样wg,消耗cmol·L-1NH4Fe(SO4)2标准溶液VmL,则TiO2质量分数表达式为____________。
(6)判断下列操作对配制NH4Fe(SO4)2标准溶液的影响(填“偏高”、“偏低”或“无影响”)
①若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,将导致结果______。
②若定容时俯视容量瓶刻线,将导致结果_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验中需用2.0mol/L的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分别为
A.1000mL,212gB.950mL,201.4gC.100mL,21.2gD.500mL,100.7g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列条件中,两种气体所含原子数一定相等的是( )
A.同质量、不同密度的N2和CO
B.同温度、同体积的H2和N2
C.同体积、同密度的C2H6和NO
D.同压强、同体积的N2O和CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com