
【题目】通常状况下,在体积一定的密闭容器中的NH3和Cl2恰好完全反应,若反应产物只有N2和NH4Cl,则反应前后容器中的压强比应接近于
A.1:11B.11:1C.7:11D.1:1
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】今有下列转化关系:

(1)A、E的结构简式为:A__________________________E__________________________
(2)反应①、⑤的反应类型是①__________________⑤__________________
(3)反应③的化学方程式为:__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A.1mol任何纯净物都含有相同的原子数
B.1mol O2中约含有6.02×1023个氧气分子
C.1mol氢中含有2mol氢原子
D.阿伏加德罗常数就是6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种高分子化合物(Ⅵ)是目前市场上流行的墙面涂料之一,其合成路线如下(反应均在一定条件下进行):
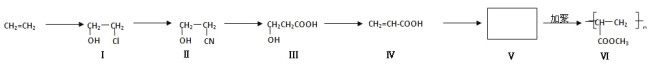
回答下列问题:
(1)化合物Ⅲ中所含官能团的名称是___________________、_______________________。
(2)化合物Ⅲ生成化合物Ⅳ的同时,副产物为____________________________。
(3)CH2=CH2与溴水反应方程式:_______________________________。
(4)写出合成路线中从化合物Ⅳ到化合物Ⅴ的反应方程式:_____________________。
(5)下列关于化合物Ⅲ、Ⅳ和Ⅴ的说法中,正确的是_____________。
A化合物Ⅲ可以发生氧化反应
B化合物Ⅲ不可以与NaOH 溶液反应
C化合物Ⅳ能与氢气发生加成反应
D化合物Ⅲ、Ⅳ均可与金属钠反应生成氢气
E化合物Ⅳ和Ⅴ均可以使溴的四氯化碳溶液褪色
(6)写出化合物Ⅰ与氧气在Cu催化下反应的产物______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某废旧铍铜元件(含BeO:25%、CuS:71%、少量FeS和SiO2)中回收铍和铜两种金属的工艺流程如下:

已知:I.铍、铝元素化学性质相似
II.常温下:Ksp[Cu(OH)2]=2.2×10-20、Ksp[Fe(OH)3]=4.0×10-38、Ksp[Mn(OH)2]=-2.1×10-13
(1)滤液A的主要成分除NaOH外,还有_____ (填化学式),写出反应I中含铍化合物与过量盐酸反应的离子方程式_____________。
(2)①溶液C中含NaCl、BeCl2和少量HCl,为提纯BeCl2,选择最合理步骤顺序______。
a.加入过量的NaOH b.通入过量的CO2 c.加入过量的氨水
d.加入适量的HC1 e.过滤 f.洗涤
②从BeCl2溶液中得到BeCl2固体的操作是________________。
(3)①MnO2能将金属硫化物中的硫元素氧化为硫单质,写出反应II中CuS 发生反应的化学方程式______________。
②若用浓HNO3溶解金属硫化物,缺点是____________(任写一条)。
(4)溶液D中含c(Cu2+)=2.2mol/L、c(Fe3+)=0.008mol/L c(Mn2+)=0.01mol/L,逐滴加入稀氨水调节pH可依次分离,首先沉淀的是___ (填离子符号),为使铜离子开始沉淀,常温下应调节溶液的pH值大于____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是现代文明的原动力,通过化学方法开辟新能源和提高能量转化率。
请回答下列问题:
(1)已知一定条件下白磷转化为红磷释放出能量,故白磷比红磷稳定性______(填“强”、“弱”)
(2)化学反应的本质是旧的化学键断裂,新的化学键形成。已知断开1molH﹣H键、1molN≡N键、lmolN﹣H键分别需要吸收的能量为436kJ、946kJ、391kJ。那么生成1mo1 NH3需要________(填“放出”或“吸收”)__________kJ 的热量。
(3)化学电源在生产生活中有着广泛的应用。
①为了探究化学反应中的能量变化,某同学设计了如下两个实验(如下图)。
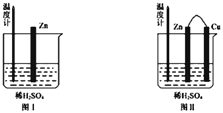
下列说法正确的是___________(填序号)
A.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面
B.图Ⅱ中产生气体的速率比Ⅰ快
C.图Ⅰ中温度计的示数高于图Ⅱ的示数
D.图Ⅰ和图Ⅱ中温度计的示数相等,且均高于室温
②燃料电池是一种高效、环境友好的供电装置。以氢气为燃料的电池中,电解质溶液为氢氧化钾溶液,负极的反应式为_______________________,当外电路转移1.2mol电子,消耗的氧气的体积为_____________ L(标准状况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会、生产、生活密切相关。下列做法值得提倡的是
A.小苏打用作净水剂B.“地沟油”加工为生物燃料
C.饮高度酒预防新冠肺炎D.漂粉精作食品漂白剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.同主族元素氢化物的稳定性,自上而下逐渐增强
B.电子结构相同的微粒,它们的化学性质亦相同
C.元素Si、P、S、C1最高价含氧酸的酸性依次增强
D.同周期的短周期元素自左而右原子半径依次增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)广泛存在于以煤为原料的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染。
(1)羰基硫的结构与二氧化碳相似,电子式为______________,硫原子的结构示意图______________
(2)羰基硫的氢解和水解反应是两种常用的脱硫方法:
氢解反应:COS(g)+H2(g)![]() H2S(g)+CO(g) ΔH1=+7kJ/mol
H2S(g)+CO(g) ΔH1=+7kJ/mol
水解反应:COS(g)+H2O(g)![]() H2S(g)+CO2(g) ΔH2=-34kJ/mol
H2S(g)+CO2(g) ΔH2=-34kJ/mol
已知:2H2(g)+O2(g)=2H2O(g) ΔH=-484kJ/mol
表示CO燃烧热的热化学方程式为________。
(3)氢解反应平衡后保持温度和压强不变通入适量的He,则正反应速率___________,COS的转化率_______(填“增大”、“减小”或“不变”)。
(4)若在绝热、恒容的密闭体系中,投入一定量COS(g)和H2(g),发生氢解反应,下列示意图能说明t1时刻反应达到平衡状态的是______(填字母序号)。(下图中υ正、K、n、m分别表示正反应速率、平衡常数、物质的量和质量)
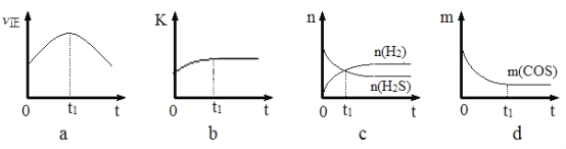
(5)某温度下,在体积为2 L密闭的容器中通入2molCOS(g)和4molH2O(g)发生上述水解反应,5 min后达到平衡,测得COS(g)的转化率是75%,回答下列问题:
①v(H2S)=________mol/(L·min)
②该温度下平衡常数K=__________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com