
【题目】铜是一种重要的战略物资,以黄铜矿(主要成分是CuFeS2)为主要原料生产铜、铁红、单质硫时,原料的综合利用率较高,其主要流程如图所示(己知Na[CuCl2]的电离方程式为:Na[CuCl2]=Na++[CuCl2]-):
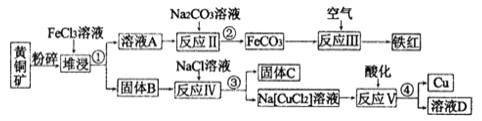
(1)流程中粉碎的目的是_____________,操作①、②、③、④的目的相同,在实验中这种操作的名称是____________。
(2)铁红的重要用途:__________________,固体B中含有两种产物,一种是单质C、另一种是原子个数比为1:l 的一种金属的低价态盐,写出堆浸时反应的化学方程式:________。
(3)反应V的离子方程式:___________________。
(4)此方法中得到的铜纯度不能满足某些生产的需要,需要利用电解法进行提纯。若用如图所示的装置进行电解精炼,则乙中溶液的溶质是_________,e电极上的电极反应式为_____。
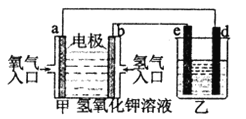
若当电路中有2mol电子通过时,乙中某个电极质量减轻了63.92g,则粗铜的纯度为(假设杂质只有铁且精炼时铜与铁的放电比例与混合物比例相同,计算时用%表示保留一位小数)____________(已知相对原子质量:Fe 56 Cu 64 )。
【答案】增大反应物间的接触面积,加快反应速率,使反应更充分过滤红色油漆和涂料CuFeS2+3FeCl3=4FeCl2+CuCl↓+2S↓2[CuCl2]ˉ=Cu+Cu2++4ClˉCuSO4Cu2++2eˉ=Cu99.1%
【解析】氯化铁具有氧化性,能氧化黄铜矿,根据(2)中提示,固体B中含有两种产物,一种是单质C、另一种是原子个数比为1:l 的一种金属的低价态盐,可知反应①为CuFeS2+3Fe3++Cl-=4Fe2++CuCl↓+2S↓,然后过滤得到固体CuCl和S和滤液,向滤液中加入碳酸钠发生反应Ⅱ,发生的离子反应方程式为Fe2++CO32-=FeCO3↓,过滤得到FeCO3,在空气中灼烧FeCO3得到氧化铁,反应Ⅲ为4FeCO3+O2 ![]() 2Fe2O3+4CO2;向CuCl、S的混合物中加入NaCl溶液,发生反应Ⅳ为Cl-+CuCl=[CuCl2]-,过滤得到Na[CuCl2],再加入水发生反应V生成Cu和溶液D,Cu+在反应V中发生自身氧化还原反应,歧化为Cu2+和Cu,则D为CuCl2、NaCl。
2Fe2O3+4CO2;向CuCl、S的混合物中加入NaCl溶液,发生反应Ⅳ为Cl-+CuCl=[CuCl2]-,过滤得到Na[CuCl2],再加入水发生反应V生成Cu和溶液D,Cu+在反应V中发生自身氧化还原反应,歧化为Cu2+和Cu,则D为CuCl2、NaCl。
(1)将矿石粉碎,可以增大与氯化铁溶液的接触面积,从而加快反应速率;根据流程图,操作①、②、③、④都是过滤,故答案为:增大反应物间的接触面积,加快反应速率,使反应更充分;过滤;
(2)铁红常用作红色油漆和涂料;固体B中含有CuCl和S,堆浸时反应的化学方程式为CuFeS2+3FeCl3=4FeCl2+CuCl↓+2S↓,故答案为:CuFeS2+3FeCl3=4FeCl2+CuCl↓+2S↓;
(3)反应V的离子方程式为2[CuCl2]ˉ=Cu+Cu2++4Clˉ,故答案为:2[CuCl2]ˉ=Cu+Cu2++4Clˉ;
(4)电解精炼铜,用粗铜作阳极,精铜作阴极,硫酸铜溶液作电解质溶液;根据图示,通入氢气的为负极,则 e电极为阴极,发生还原反应,电极反应式为Cu2++2eˉ=Cu;设粗铜中反应的铜的物质的量为x,铁为y,阳极反应为Cu-2eˉ=Cu2+、Fe-2eˉ= Fe 2+,则2x+2y=2mol,64x+56y=63.92g,解得x=0.99mol,y=0.01mol,粗铜的纯度为![]() ×100%=99.1%,故答案为:CuSO4 ;Cu2++2eˉ=Cu;99.1%。
×100%=99.1%,故答案为:CuSO4 ;Cu2++2eˉ=Cu;99.1%。


科目:高中化学 来源: 题型:
【题目】【2017孝义市模拟】下列储存药品的方法中,正确的是( )
A.液溴保存在带橡胶塞的玻璃瓶中
B.新制氯水保存在棕色广口瓶中
C.金属锂保存在石蜡油中
D.硅酸钠溶液保存在带磨口玻璃塞的玻璃瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2015北京理综化学】最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:
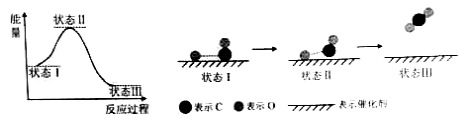
下列说法中正确的是 ( )
A.CO和O生成CO2是吸热反应
B.在该过程中,CO断键形成C和O
C.CO和O生成了具有极性共价键的CO2
D.状态Ⅰ →状态Ⅲ表示CO与O2反应的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知25 ℃时有关弱酸的电离平衡常数:
弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
电离平衡常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
① 同温度下,等pH值的a. NaHCO3、b. NaCN、c.Na2CO3溶液的物质的量浓度由大到小的顺序为__________(填序号)。
② 25 ℃时,将20mL 0.1mol/LCH3COOH溶液和20mL0.1mol/LHSCN溶液分别与20ml0.1mol/L NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示:
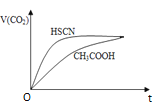
反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是:________反应结束后所得两溶液中,c(SCN-)________c(CH3COO-)(填“> ”、“< ”或“= ”)
③ 若保持温度不变,在醋酸溶液中加入一定量氨气,下列量会变小的是______(填序号)。
a.c(CH3COO-) b.c(H+) c.Kw d.醋酸电离平衡常数
(2)煤燃烧产生的烟气也含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。己知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867.0kJ mol-1
2NO2(g)![]() N2O4(g) △H=-56.9kJ mol-1
N2O4(g) △H=-56.9kJ mol-1
H2O(g)=H2O(l) △H=-44.0kJ mol-1
写出CH4催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(l)的热化学方程式_________
(3)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50mL 2mol/L的氯化铜溶液的装置示意图:请回答下列问题:
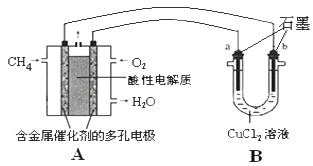
①甲烷燃料电池的负极反应式是____________
② 当A中消耗0.15mol氧气时.B 中____极增重_______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把SO2通入Fe(NO3)3溶液中,溶液由黄色变为浅绿色,但立即又变为黄色,此时若滴入BaCl2溶液,则会产生白色沉淀。在上述一系列变化过程中,最终被还原的是( )
A.SO2 B.NO3- C.Fe3+ D.Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下关于甲烷的说法中错误的是( )
A.甲烷分子具有正四面体结构
B.甲烷化学性质比较稳定,不被任何氧化剂氧化
C.甲烷分子中具有极性键
D.甲烷分子中四个C﹣H键是完全等价的键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铁为阳极,铜为阴极,对足量的NaOH溶液进行电解,一段时间后得到2 mol Fe(OH)3沉淀。此过程中共消耗水 ( )
A.3 mol B.4 mol C.5 mol D.6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对元素周期律和元素周期表的认识正确的是( )
A. 元素周期律的本质是随着核电荷数的增加元素化合价呈周期性的变化
B. 核外电子排布的周期性变化是元素性质周期性变化的本质
C. 元素周期表中可以把元素分成s、p、d、ds四个区
D. 元素周期表中最外层电子数<2的元素一定是金属元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com