
| A. | 塑料,合成纤维和合成橡胶都是合成材料 | |
| B. | 煤是由有机物和无机物组成的复杂混合物 | |
| C. | 聚乙烯是通过聚反应制得的高分子化合物 | |
| D. | 钠,铝与铁通常都是采用电解法冶铁的 |
分析 A.三大合成材料是合成塑料、合成橡胶、合成纤维;
B.煤是一种复杂的混合物,主要含碳元素,还含有氢元素和少量的氮、硫、氧等元素;
C.乙烯发生加聚反应生成聚乙烯;
D.电解法:冶炼活泼金属K、Ca、Na、Mg、Al,一般用电解熔融的氯化物(Al是电解熔融的Al2O3)制得;
热还原法:冶炼较不活泼的金属Zn、Fe、Sn、Pb、Cu,常用还原剂有(C、CO、H2等);
热分解法:冶炼不活泼的金属Hg、Ag用加热分解氧化物的方法制得.
解答 解:A.以煤、石油和天然气为主要原料可制造化工产品、合成塑料、合成橡胶、合成纤维等,故A正确;
B.煤是一种不可再生的资源,是由长期埋在地层中的古代植物的遗体形成的,主要含碳元素,还含有氢元素和少量的氮、硫、氧等元素,是一种复杂的混合物,故B正确;
C.乙烯发生加聚反应生成聚乙烯,所以聚乙烯是乙烯的加聚反应后生成的高分子聚合物,故C正确;
D.Fe用热还原法冶炼,故D错误;
故选D.
点评 本题考查了汽油、煤、聚乙烯、金属冶炼等相关知识点,掌握它们的性质是解答的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 容器 | 起始各物质的物质的量/mol | 达到平衡时体系 能量的变化 | |||
| SO2 | O2 | SO3 | Ar | ||
| 甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2 |
| 丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
| A. | Q1=Q2=Q3 | |
| B. | 达到平衡时,丙容器中SO2的体积分数最大 | |
| C. | 甲、乙、丙3个容器中反应的平衡常数不相等 | |
| D. | 若在上述条件下反应生成2molSO3(s)的放热大于197kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冬天气温低,反应速率降低,对环境污染会更大 | |
| B. | 改变压强对反应速率没有影响 | |
| C. | 使用催化剂能促使反应正向进行 | |
| D. | 无论外界条件怎样改变,均对此化学反应的速率无影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
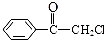 苯氯乙酮是一具有荷花香味且有强催泪作用的化学试剂,它的结构简式如图所示,则苯氯乙酮不可能具有的化学性质是ce(填字母序号).
苯氯乙酮是一具有荷花香味且有强催泪作用的化学试剂,它的结构简式如图所示,则苯氯乙酮不可能具有的化学性质是ce(填字母序号).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 羟甲基(-CH2OH)和甲氧基(CH3O-) | B. | S2-和Cl- | ||
| C. | Mg2+和F- | D. | 羟基(-OH)和氢氧根(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴定前滴定管尖嘴内无气泡,终点读数时有气泡,则测定结果偏小 | |
| B. | 滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定 | |
| C. | 用酚酞作指示剂,当锥形瓶中溶液由粉红色变无色时停止滴定 | |
| D. | 滴定时两眼应注视滴定管中液面的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CCl4可由CH4制得,可用于萃取碘水中的碘 | |
| B. | 乙醇、乙酸和乙酸乙酯能用饱和碳酸钠溶液鉴别 | |
| C. | 煤油可由石油分馏获得,可用作燃料和保存少量金属钠 | |
| D. | 蒸馏装置中,温度计的水银球应插入到混合溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 298K时,某容积固定为1L的密闭容器中发生如下可逆反应:A(g)?2B(g)△H=akJ•mol-1.其中B的物质的量浓度随时间变化如图所示.试回答下列问题.
298K时,某容积固定为1L的密闭容器中发生如下可逆反应:A(g)?2B(g)△H=akJ•mol-1.其中B的物质的量浓度随时间变化如图所示.试回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com