
| A. | 常用明矾或硫酸铝做净水剂 | |
| B. | 实验室将氯化铁晶体溶于浓盐酸来配制饱和氯化铁溶液 | |
| C. | 用热的纯碱液清洗餐具表面的油污比用冷的溶液效果好 | |
| D. | 泡沫灭火器中用NaHCO3溶液和Al2(SO4)3溶液发生反应产生CO2 |
分析 A、常用明矾或硫酸铝做净水剂,是用铝离子的水解生成氢氧化铝胶体;
B、实验室将氯化铁晶体溶于浓盐酸来配制饱和氯化铁溶液,浓盐酸对铁离子的水解起抑制作用;
C、盐 的水解是吸热过程;
D、NaHCO3溶液和Al2(SO4)3溶液混合两者水解相互促进;
解答 解:A、常用明矾或硫酸铝做净水剂,是用铝离子的水解生成氢氧化铝胶体,无需要抑制,故A不选;
B、实验室将氯化铁晶体溶于浓盐酸来配制饱和氯化铁溶液,浓盐酸对铁离子的水解起抑制作用,符合条件,故B选;
C、盐 的水解是吸热过程,所以热的纯碱液清洗餐具表面的油污比用冷的溶液效果好的原因是加热对碳酸根离子的水解起促进作用,故C不选;
D、NaHCO3溶液和Al2(SO4)3溶液混合两者水解相互促进,而不是抑制,故D不选;
故选B.
点评 本题考查了盐类水解,结合“谁强谁显性、谁弱谁水解”,根据水解平衡的移动来分析解答即可,题目难度不大.


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:解答题
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
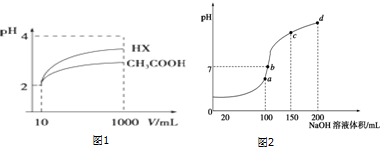
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
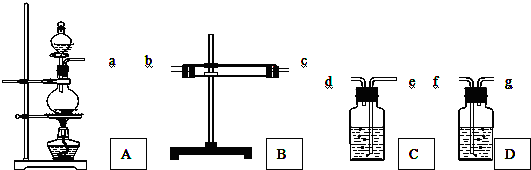
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 给试管内液体加热时,液体体积不应超过试管容积的$\frac{1}{3}$ | |
| B. | 过滤、蒸发操作过程中都需要用玻璃棒不断搅拌液体 | |
| C. | 测定某溶液的pH将干燥试纸浸入到待测溶液,过一会儿取出,与标准比色卡比较 | |
| D. | 用容量瓶配置一定物质的量浓度溶液时,容量瓶必须干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,0.1 mol•L-1 HA溶液的pH=3,则HA的电离:HA=H++A- | |
| B. | 向硫酸铵溶液中加入适量氨水,当溶液呈酸性时,溶液中c(SO42-)=c(NH4+) | |
| C. | 向1 mL 2 mol•L-1NaOH溶液中滴加1~2滴0.1 mol•L-1MgCl2溶液后,再滴加2滴0.1 mol•L-1 FeCl3溶液:Mg2++2OH-=Mg(OH)2↓,3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ | |
| D. | 浓度相等的①NH4HSO4②NH4C1③(NH4)2SO4溶液中,c(NH4+)的大小顺序为③>①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

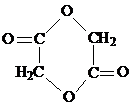 .
.


 (任写其中一种).
(任写其中一种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸钡不溶于水,所以硫酸钡是非电解质 | |
| B. | 二氧化碳溶于水可以导电,所以,二氧化碳是电解质 | |
| C. | 固态磷酸是电解质,所以磷酸在熔化时或溶于水时都能导电 | |
| D. | 液态氯化氢不能导电,但氯化氢是电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com