
【题目】(13分)卤水中含有丰富的镁离子,可制取多种含镁产品。
(1)向卤水中加入Ca(OH)2制取Mg(OH)2,其离子方程式是 。
(2)Mg(OH)2可制取MgO,进而制得金属镁。
①灼烧Mg(OH)2得到MgO的化学方程式是______。
②1200℃,真空条件下用硅铁(含硅单质95~99%)将MgO还原为镁蒸汽(铁不参与反应),其原理可用化学方程式表示为______。
(3)Mg(OH)2可用来制取MgCl2,进而制取金属镁。
①从MgCl2溶液得到MgCl26H2O的操作是______、过滤。
②MgCl26H2O与SOCl2混合后加热,可获得无水MgCl2(已知SOCl2与水接触时迅速形成白雾,生成SO2)。得到无水MgCl2的化学方程式是______。
(4)Mg(OH)2还可用来制取三硅酸镁(xMgO3SiO2)。三硅酸镁是医疗上某抗酸药的主要成分。已知硅酸盐的化学式通常用氧化物形式表示,如石棉CaMg3Si4O12表示为3MgOCaO4SiO2。
①三硅酸镁中和胃酸的离子方程式是:xMgO3SiO2+□H+=□Mg2++□SiO2+□___
②为确定xMgO3SiO2中x值。取三硅酸镁样品0.52 g,加入0.5000 mol/LH2SO4标准液15.00 mL,充分反应后,用0.5000 mol/L的NaOH标准液滴定过量的H2SO4,消耗NaOH标准液14.00 mL。则x=______。
【答案】(1)Mg2++2OH-=Mg(OH)2↓或Mg2++Ca(OH)2=Mg(OH)2↓+Ca2+(2分)
(2)①Mg(OH)2 ![]() MgO+H2O (1分)
MgO+H2O (1分)
②Si+2MgO![]() 2Mg↑+SiO2 (2分)
2Mg↑+SiO2 (2分)
(3)①加热浓缩、降温结晶(2分)
②6SOCl2+MgCl26H2O![]() MgCl2+6SO2↑+12HCl↑(2分)
MgCl2+6SO2↑+12HCl↑(2分)
(4)①2x x 3 xH2O(2分)
②2(2分)
【解析】
试题分析:(1)制备氢氧化镁,即是利用Mg2+与OH-反应,方程式为:Mg2++2OH-=Mg(OH)2↓;
(2)①灼烧氢氧化镁,生成氧化镁即Mg(OH)2 ![]() MgO+H2O ;②根据提示可知,Si单质与MgO在1200℃条件下生成Mg,方程式为:Si+2MgO
MgO+H2O ;②根据提示可知,Si单质与MgO在1200℃条件下生成Mg,方程式为:Si+2MgO![]() 2Mg↑+SiO2 ;
2Mg↑+SiO2 ;
(3)①使溶液结晶需要 加热浓缩、降温结晶;②根据提示可得到:6SOCl2+MgCl26H2O![]() MgCl2+6SO2↑+12HCl↑;
MgCl2+6SO2↑+12HCl↑;
(4)①根据提示可将反应配平:xMgO3SiO2+2xH+=xMg2++3SiO2+xH2O② 首先可以计算出三硅酸镁消耗H+的物质的量为:n(H+)=2n(H2SO4)-n(NaOH)=![]() =0.008mol;根据物质的量之比等于系数之比,可得到:n(xMgO3SiO2):n(H+)=1:2x=
=0.008mol;根据物质的量之比等于系数之比,可得到:n(xMgO3SiO2):n(H+)=1:2x=![]() 解得x=2。
解得x=2。


科目:高中化学 来源: 题型:
【题目】未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列符合未来新能源标准的是( )
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物能 ⑦风能 ⑧氢能
A. ①②③④ B. ⑤⑥⑦⑧ C. ③⑤⑦ D. ③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质的比较中,正确的是
①沸点:H2O>HCl>HF ②密度:四氯化碳>水>汽油
③酸性:H3PO4>H2SO4>HClO4④离子半径:O2->F->Na+
A.①③B.②④C.①④D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实,不能用勒夏特列原理解释的是( )
A. 溴水中有平衡:Br2+H2O![]() HBr+ HBrO加入 AgNO3溶液后,溶液颜色变浅
HBr+ HBrO加入 AgNO3溶液后,溶液颜色变浅
B. 对CO(g)+ NO2(g)![]() CO2(g)+NO(g)平衡体系增大压强可使颜色变深
CO2(g)+NO(g)平衡体系增大压强可使颜色变深
C. 升高温度能够增大硝酸钾在水中的溶解度
D. 合成 NH3反应,为提高 NH3的产率,理论上应采取相对较低温度的措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向200mL 某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,充分反应测得最后溶液的pH>7。
(1)此时溶液的溶质如果是单一成分,可能是___________;如果是多种成分,可能是__________。
(2)在上述所得溶液中,逐滴缓慢滴加2 mol·L-1的盐酸,所得气体(不考虑溶解于水)的体积与所加盐酸的体积关系如图所示:
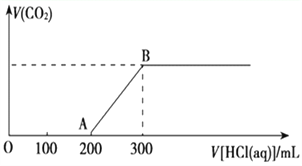
①加入盐酸200 mL之前,无气体产生,写出OA段发生反应的离子方程式:_______。
②B点时,反应所得溶液中溶质的物质的量浓度是_________ (溶液体积的变化忽略不计)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com