
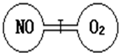
 如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同.已知2NO+O2═2NO2,打开活塞,使NO与O2充分反应,则下列说法错误的是( )
如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同.已知2NO+O2═2NO2,打开活塞,使NO与O2充分反应,则下列说法错误的是( )| A. | 开始时左右两室分子数相同 | B. | 反应开始后NO室压强减小 | ||
| C. | 最终容器内密度与原来相同 | D. | 最终容器内仍然有O2存在 |
分析 A、由左右两室体积相同,两容器内气体密度相同可知,两容器中气体的质量一定相等,再结合n=$\frac{m}{M}$进行判断气体的物质的量关系,据此判断;
B、发生2NO+O2=2NO2,反应后总的物质的量减少,故反应后NO室的气体物质的量要减小;
C、气体的总质量为原来一氧化氮与氧气质量之和,为NO质量的2倍,体积为左右两室的体积之和,为左室的2倍,故密度不变;
D、NO、O2的质量相等,二者物质的量之比为32:30=16:15,发生2NO+O2=2NO2,O2过量.
解答 解:A、由左右两室体积相同,两容器内气体密度相同可知,两容器中气体的质量一定相等,而NO和O2的摩尔质量不相等,故其物质的量不相等,开始时左右两室分子数不相同,故A错误;
B、发生2NO+O2=2NO2,反应后总的物质的量减少,平均充满左右两室,故反应后NO室的气体物质的量要减小,故压强减小,故B正确;
C、反应后气体的总质量为原来一氧化氮与氧气质量之和,为NO质量的2倍,体积为左右两室的体积之和,为左室的2倍,故密度不变,故C正确;
D、NO、O2的质量相等,二者物质的量之比为32:30=16:15,发生2NO+O2=2NO2,O2过量,故最终容器内有O2存在,故D正确;
故选A.
点评 本题考查阿伏伽德罗定律及推论、化学计算等,难度中等,注意二者发生反应物质的量减少,掌握基础是关键.


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源:2016-2017学年山东省高一上10月月考化学试卷(解析版) 题型:推断题
甲、乙、丙均为化合物,其中甲为淡黄色的固体,乙常温下为无色无味液体,丙为常见的无色无味气体。它们有如下图的转化关系,已知D为黄绿色气体,按要求回答下列问题:

(1)甲物质为_____________(填化学式)。
(2)1mol乙和足量甲反应可生成______________mol B物质;1mol丙和足量甲反应可生成____________mol B物质。
(3)D能使湿润的有色布条褪色,其褪色原因是_______________。(结合化学反应方程式描述原因)
(4)丙与溶液F反应的化学方程式为_____________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:选择题
酸在溶剂中的电离实质是酸中的H+转移给溶剂分子,如HCl + H2O = H3O+ + Cl-。已知H2SO4和HNO3在冰醋酸中的电离平衡常数Ka1(H2SO4) = 6.3 × 10-9 ,Ka(HNO3) = 4.2 × 10-10。 下列说法正确的是
A.冰醋酸中H2SO4的电离方程式:H2SO4 + 2CH3COOH = SO42-+ 2CH3COOH2+
B.H2SO4的冰醋酸溶液中:c(CH3COOH2+) = c(HSO4-)+ 2c(SO42-) + c(CH3COO-)
C.浓度均为0.1mol·L-1的H2SO4或HNO3的冰醋酸溶液:pH(H2SO4)> pH(HNO3)
pH(HNO3)
D.向HNO3的冰醋酸溶液中加入冰醋酸,c(CH3COOH2+)/c(HNO3)减小
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:3 | C. | 3:2 | D. | 1:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 催化剂可以加快化学反应速率,也能增大化学反应的焓变 | |
| B. | 常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同 | |
| C. | 25℃下,在NH3•H2O稀溶液中加水稀释,$\frac{c({H}^{+})•c(N{H}_{3}•{H}_{2}O)}{c(N{{H}_{4}}^{+})}$的值不变 | |
| D. | 在NaHS溶液中,滴入少量CuCl2溶液产生黑色沉淀,HS-电离程度减小 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:填空题
在一个容积固定的反应器中,有一可左右滑动的密封隔板,左、右两侧分别进行如下可逆反应:2SO2(g)+O2(g) 2SO3(g);3Fe
2SO3(g);3Fe (s)+4H2O(g)
(s)+4H2O(g) Fe3O
Fe3O 4(g)+4H2(
4(g)+4H2( g)。左侧中加入SO2、O2、SO3的物质的量分别为x mol、3.25mol、1mol;右侧中加入9 mol的水蒸气和适量的铁粉(忽略铁粉对容器体积的影响)。当x在一定范围内变化时,均可以通过调节反应器的温度,使两侧反应都达到平衡,并且隔板恰好处于反应器位置2处。请填写以下空白:
g)。左侧中加入SO2、O2、SO3的物质的量分别为x mol、3.25mol、1mol;右侧中加入9 mol的水蒸气和适量的铁粉(忽略铁粉对容器体积的影响)。当x在一定范围内变化时,均可以通过调节反应器的温度,使两侧反应都达到平衡,并且隔板恰好处于反应器位置2处。请填写以下空白:
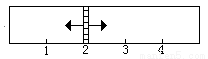
(1)若x=1.5,则左侧反应在起始时向__________(填“正”或“逆”)反应方向进行。欲使反应维持向该方向进行,则x的取值范围是______________。
(2)若x=2,平衡时混合气中SO2所占的体积分 数为______________。欲使起始反应维持向该方向进行,则x的最大值应小于____________。
数为______________。欲使起始反应维持向该方向进行,则x的最大值应小于____________。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用合适的催化剂可大大提高生产效率 | |
| B. | 由反应需在300℃进行,可知该反应是吸热反应 | |
| C. | 增大原料气中CO2的百分含量,可以提高H2的转化率 | |
| D. | 70MPa的压力,不仅可以增加单位时间内的产出,还可以提高CO2和H2的利用率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com