
萤火虫发光前后物质的变化如下:
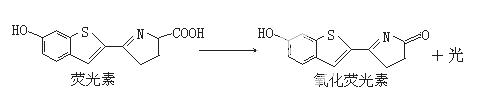
下列关于荧光素和氧化荧光素的叙述不正确的是( )
A. 二者的分子组成相差一个CHO
B.二者的分子组成相差一个CH2O
C.都能使酸性KMnO4溶液褪色
D.都既能发生加成反应又能发生取代反应
科目:高中化学 来源: 题型:
某工业废水仅含下表中的某些离子,且各种离子的物质的量浓度相等,均为0.1 mol/L(此数值忽略水的电离及离子的水解)。
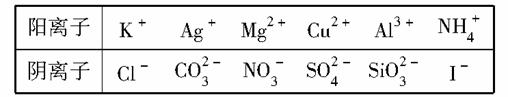
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.取该无色溶液5 mL,滴加一滴氨水有沉淀生成,且离子种类增加。
Ⅱ.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰。
Ⅲ.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是________。
(2)Ⅲ中加入盐酸生成无色气体的离子方程式是________________。
(3)甲同学最终确定原溶液中所含阳离子有________,阴离子有______;并据此推测原溶液应该呈________性,原因是________________________
(请用离子方程式说明)。
(4)另取100 mL原溶液,加入足量的NaOH溶液,此过程中涉及的离子方程式为________________。充分反应后过滤,洗涤,灼烧沉淀至恒重,得到的固体质量为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
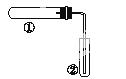
用如图装置(夹持、加热装置已略)进行实验,由②中现象,不能证实①中反应发生的是( )
| ①中实验 | ②中现象 | |
| A | 铁粉与水蒸气加热 | 肥皂水冒泡 |
| B | 加 的混合物 | 酚酞溶液变红 |
| C | NaHCO3固体受热分解 | 澄清石灰水变浑浊 |
| D | 石蜡油在碎瓷片上受热分解 | Br2的CCl4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
为了将混有K2SO4、MgSO4的KNO3固体提纯,并制得纯净的KNO3溶液 ,某学生设计如下实验方案:
,某学生设计如下实验方案:

(1)操作①为____________________。
(2)操作②~④加入的试剂依次可以为____________________________________。
(3)如何判断SO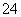 已除尽?_____________________________________________。
已除尽?_____________________________________________。
(4)实验过程中产生的多次沉淀________(填“需要”或“不需要”)多次过滤,其理由是
_____________ ____________________________________________
____________________________________________ _______________。
_______________。
(5)该同学的实验设计方案是否严密?请说明理由:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
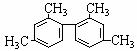
已知碳碳单键可以绕键轴自由旋转,结构简式为如下图所示的烃,下列说法中正确的是
A.分子中至少有9个碳原子处于同一平面上
 B.分子中至少有10个碳原子处于同一平面上
B.分子中至少有10个碳原子处于同一平面上
C.分子中至少有11个碳原子处于同一平面上
D.该烃属于苯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3、MgO、CaO等,生产工艺流程示意如下:

(1)将菱锌矿研磨成粉的目_________。
(2)完成“氧化除铁”步骤中反应的离子方程式:
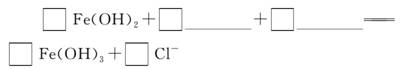
(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,化学式量为89,化学式是____________________。
(4)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为__________________。
| Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 | |
| 开始沉淀的pH | 10.4 | 6.4 | — | — |
| 沉淀完全的pH | 12.4 | 8.0 | — | — |
| 开始溶解的pH | — | 10.5 | — | — |
| Ksp | 5.6×10-12 | — | 6.8×10-6 | 2.8×10-9 |
(5)工业上从“滤液3”制取MgO过程中,合适的反应物是________(选填序号)。
a.大理石粉 b.石灰乳
c.纯碱溶液 d.烧碱溶液
(6)“滤液4”之后的操作依次为________、________、过滤、洗涤、干燥。
(7)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于________。
查看答案和解析>>
科目:高中化学 来源: 题型:
铁及其化合物与生产、生活关系密切。
(1)下图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。

①该电化腐蚀称为 。
②图中A、B、C、D四个区域,生成铁锈最多的是 (填字母)。
(2)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:

①步骤I若温度过高,将导致硝酸分解。硝酸分解的化学方程式为 。
②步骤Ⅱ中发生反应:4Fe(NO3)2+O2+(2n+4)H2O=2Fe2O3·nH2O+8HNO3,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,该反应的化学方程式为 。
③上述生产流程中,能体现“绿色化学”思想的是 (任写一项)。
(3)已知t℃时,反应FeO(s)+CO(g) Fe(s)+CO2(g)的平衡常数K=0.25。
Fe(s)+CO2(g)的平衡常数K=0.25。
①t℃时,反应达到平衡时n(CO):n(CO2)= 。
②若在1 L密闭容器中加入0.02 mol FeO(s),并通入xmolCO,t℃时反应达到平衡。此时FeO(s)转化率为50%,则x= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
加碘食盐中加入的碘酸钾是一种白色结晶粉末,常温下性质稳定,加热至560 ℃开始分解。在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应。工业生产碘酸钾的流程如下:
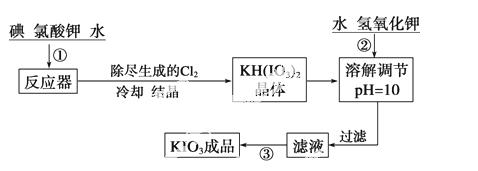
(1)已知步骤①反应器发生的反应中,单质碘和氯酸钾的物质的量之比为6∶11,则反应器中发生反应的化学方程式为
_____________________________________________________________________。
(2)步骤②中调节pH=10的目的是_______________________________________。
参照碘酸钾的溶解度:
| 温度/℃ | 20 | 40 | 60 | 80 |
| KIO3 g/100 g H2O | 8.08 | 12.6 | 18.3 | 24.8 |
操作③的方法是_____________________________________________________。
(3)检验加碘食盐中的碘元素,学生甲利用碘酸钾与碘化钾在酸性条件下发生反应,然后用四氯化碳检验生成的碘单质时,甲应观察到的明显现象有_______________________________________________________________________。
学生乙对纯净的NaCl进行了如下实验:取1 g纯净的NaCl,加3 mL水配成溶液,然后滴入5滴淀粉溶液和1 mL 0.1 mol·L-1 KI溶液,振荡,溶液无变化,然后再滴入1滴1 mol·L-1的H2SO4,振荡,一段时间后溶液变浅蓝色。请推测实验中产生蓝色现象的可能原因,用离子方程式表示
______________________________________________________________________。
(4)学生丙查阅有关食品碘强化剂的资料后知道,碘酸钙也是一种允许使用的食品碘强化剂,它是一种白色结晶或结晶性粉末,难溶于水和乙醇。丙同学在氯化钙溶液中加入理论量的碘酸钾溶液,反应生成的沉淀经水洗后,室温下干燥得碘酸钙晶体,加热至160~540 ℃变成无水物,此时固体质量为原晶体质量的78.3%,写出制备碘酸钙晶体的离子方程式:_________________________________________________;
检验沉淀已经洗涤干净的方法是_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于空气的说法中,错误的是
A.工业上利用氧气和氮气密度不同,从液态空气中分离出氧气和氮气
B.空气是一种十分重要的天然资源
C.按体积分数计,空气中约含有氮气78%、稀有气体0.94%
D.空气中敞口放置的石灰水表面出现了一层白膜是因为空气中含有二氧化碳
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com