
| A. | 酸雨有很大的危害,应提倡工厂使用清洁能源,减少CO2的排放 | |
| B. | 木材浸过水玻璃后,具有良好的防火性能 | |
| C. | 烧碱和纯碱都属于碱 | |
| D. | 氯气泄漏后,人应逆风且往低处跑 |
分析 A.酸雨与N、S的氧化物有关;
B.水玻璃为硅酸钠溶液,不燃烧、不支持燃烧;
C.纯碱为碳酸钠;
D.氯气的密度比空气密度大,有毒.
解答 解:A.酸雨与N、S的氧化物有关,与二氧化碳的排放无关,故A错误;
B.水玻璃为硅酸钠溶液,不燃烧、不支持燃烧,则木材浸过水玻璃后,具有良好的防火性能,故B正确;
C.纯碱为碳酸钠,属于盐,而烧碱为NaOH,属于碱,故C错误;
D.氯气的密度比空气密度大,有毒,则氯气泄漏后,人应逆风且往高处跑,故D错误;
故选B.
点评 本题考查三废处理及环境保护,为高频考点,把握物质的性质、环境污染物及环保为解答的关键,侧重分析与应用能力的考查,注意化学与生活的联系,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 2个甲基,能生成4种一氯代物 | B. | 3个甲基,能生成5种一氯代物 | ||
| C. | 4个甲基,能生成4种一氯代物 | D. | 4个甲基,能生成5种一氯代物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在燃煤时加入适量石灰石,可减少 SO2的排放:2CaCO3+O2+2SO2═2CaSO3+2CO2 | |
| B. | 自然界各种原生铜的硫化物经氧化、淋滤作用后产生的硫酸铜,遇到难溶液的 PbS,慢慢转变为铜蓝(CuS):Cu2++SO42-+PbS═CuS+PbSO4 | |
| C. | 向海带灰浸出液中加入硫酸、双氧水:2I-+2H++H2O2═I2 +2H2O | |
| D. | 在盐碱地(含较多 NaCl、Na2CO3)上通过施加适量 CaSO4,可降低土壤的碱性:CaSO4+Na2CO3═CaCO3↓+Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阴离子的半径:Y>W | |
| B. | 气态氢化物稳定性:Y>Z | |
| C. | 最外层电子数:Y=Z | |
| D. | X、Y、Z中的两种元素形成的化合物在常温下都为气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 操作 | 现象 |
| A | BaSO3难溶于水 | 将SO2通入Ba(NO3)2溶液中 | 有白色沉淀生成 |
| B | 验证非金属性:Br>I | 将溴水滴加到淀粉KI溶液中 | 溶液变蓝 |
| C | 验证SO2的漂白性 | 将SO2通入酸性KMnO4溶液中 | KMnO4溶液褪色 |
| D | 验证某化合物一定是钠盐 | 该化合物在酒精灯上灼烧 | 焰色为黄色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 保持温度不变,减小压强 | B. | 保持恒温恒容,充入氦气 | ||
| C. | 其它条件不变时,升高温度 | D. | 其它条件不变时,加入少量A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2溶于水:Na2O2+H2O═2Na++2OH-+O2↑ | |
| B. | 向氧化铁中加入氢碘酸发生反应:Fe2O3+6HI═2Fe2++I2+3H2O+4I- | |
| C. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 漂白粉溶液中通入过量的CO2:ClO-+CO2+H2O═HClO+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝镁合金的硬度较大,钠钾合金的硬度较小 | |
| B. | 因为钠的金属性比镁要强,所以钠的熔点比镁要高 | |
| C. | 镁能置换硫酸铜溶液中的铜,钠也能置换硫酸铜溶液中的铜 | |
| D. | 在空气中都能被点燃,生成的产物都是氧化物,氧在产物中的化合价都是-2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
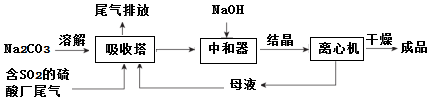
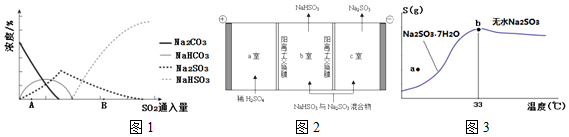
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com