
如下图所示的原电池,一段时间后某极析出1.28克的固体。求:
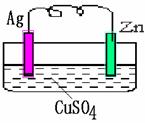
|
科目:高中化学 来源:2012届浙江省东阳中学高三下学期阶段检测化学试卷 题型:单选题
控制适合的条件,KI溶液过量,将反应
2Fe3++2I-=2Fe2++I2设计成如下图所示的原电池。下列判断正确的是 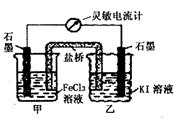
| A.反应开始时,甲中石墨电极上Fe3+发生氧化反应 |
| B.反应开始时,乙中石墨电极的反应式:I2+2e-=2I- |
| C.电流计读数为零时,在甲中加入KSCN溶液,出现血红色 |
| D.电流计读数为零时,反应处在停止状态 |
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省沈阳市高二上教学质量监测化学试卷(解析版) 题型:填空题
I.现将反应2Fe3+ + 2I-  2Fe2+ + I2设计成如下图所示的原电池
2Fe2+ + I2设计成如下图所示的原电池

(1)能说明反应达到平衡的标志是__________;(填序号)
a.电流计读数为零
b.电流计指针不再偏转且不为零
c.电流计指针偏转角度最大
(2)若盐桥中装有琼脂-饱和KCl溶液,反应过程中的Cl-移向烧杯________;(填“甲”或“乙”)
(3)反应达到平衡后,向甲中加入适量FeCl2固体,此时___________(填“甲”或“乙”)中石墨电极为负极,对应的电极反应方程式为____________________________。
II.如下图所示的装置,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。

(4)装置乙中电极F的电极反应式____________________;
(5)相同条件下,装置甲、乙的C、E电极生成物质的体积之比为____________________;
(6)欲用装置丙进行粗铜精炼,电极G应该是____________________;
(7)装置丁中电极_______附近红褐色变深,说明氢氧化铁胶粒带正电荷。
查看答案和解析>>
科目:高中化学 来源:2015届河南省高一下学期第二次阶段测试化学试卷(解析版) 题型:填空题
能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。阅读下列有关能源的材料,回答有关问题:
(1)从能量的角度看,断开化学键要吸收能量,形成化学键要放出能量。已知拆开1 mol H-H键、1 mol I-I、1 mol H-I键分别需要吸收的能量为436 kJ、151 kJ、299 kJ。则由氢气和碘单质反应(H2+I2=2HI)生成1 mol HI需要 (填“放出”或“吸收”) ___ kJ的热量。
(2)在生产和生活中经常遇到化学能与电能的相互转化。

在如图甲装置中,负极电极反应式为 ,发生的是 反应(填“氧化”或“还原”,下同)。正极电极反应式为 ;总反应的离子方程式为 。
(3)若用氢氧化钾溶液做电解质溶液,用氢气做燃料,空气做氧化剂制成燃料电池,其负极反应式为 ;正极反应式为 。当有标状下2.24L氢气消耗时,另一极消耗氧气的物质的量为 。
(4)在如下图所示的原电池中,铝做 极,导线上电子由 极流向 极。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省济宁市高三12月月考化学试卷 题型:选择题
将反应2Fe3++2I- 2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是
2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是

A.反应开始时,乙中石墨电极上发生氧化反应
B.电流计读数为零时,达到化学平衡状态
C.乙池中若换为Fe电极和FeCl2溶液,则电流计指针向相
反方向偏转
D.电流计读数为零后,在甲中溶入FeCl3固体,乙中石墨电极仍为负极
查看答案和解析>>
科目:高中化学 来源:2011-2012学年吉林省吉林市高三上学期期末考试化学试卷 题型:选择题
实验发现,298K时,在FeCl3酸性溶液中加入少量锌粒后,Fe3+立即被还原成Fe2+。某化学兴趣小组根据该实验事实设计了如下图所示的原电池装置。下列有关说法中正确的是
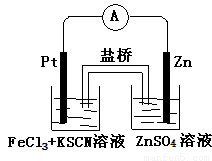
A.该原电池的正极反应是:Zn—2e-=Zn2+
B.左烧杯中溶液的红色逐渐褪去
 C.该电池铂电极上有气泡出现
C.该电池铂电极上有气泡出现
D.该电池总反应为:3Zn + 2Fe3+ = 2Fe + 3Zn2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com