
下列做法与所实现的目标,正确的是( )
A.回收电子垃圾通过高温焚烧熔出金属,可实现资源循环利用和绿色环保
B.回收废弃塑料制成燃油替代汽、柴油,可减轻环境污染和节约化石能源
C.采用天然石材装修家居,可减轻室内甲醛等有机物和放射性物质的污染
D.将工业废水加压排放到地下深井,可实现自然过滤净化和避免水的污染
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.Li是最活泼金属,F是最活泼非金属
B.Mg(OH)2碱性比Ca(OH)2强
C.元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行
D.X2+的核外电子数目为18,则X在第四周期第ⅡA族
查看答案和解析>>
科目:高中化学 来源: 题型:
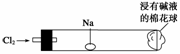
“绿色化学实验”进课堂,某化学老师为“氯气与金属钠反应”设计了如右图所示装置与操作以替代相关的课本实验。实验操作:钠与氯气反应的装置可作如图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆大的金属钠(已擦净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是( )
A.反应生成的大量白烟是氯化钠晶体
B.玻璃管尾部塞一团浸有NaOH溶液的棉花球是用于吸收过量的氯气,以免其污染空气
C.钠着火燃烧产生苍白色火焰
D.若在棉花球外沿滴一滴淀粉碘化钾溶液,可据其颜色变化判断氯气是否被碱液完全吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各项与化学平衡移动原理无关的是 ( )。
A.收集氯气用排饱和食盐水的方法
B.加催化剂,使N2和H2在一定的条件下转化为NH3
C.可用浓氨水和氢氧化钠固体快速制取氨气
D.加压条件下有利于SO2和O2反应生成SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒温恒压下,向密闭容器中充入4 mol SO2和2 mol O2,发生如下反应:2SO2(g)+O2(g)2SO3(g) ΔH<0。2 min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量Q kJ。则下列分析正确的是 ( )。
A.在该条件下,反应前后的压强之比为6∶5.3
B.若反应开始时容器体积为2 L,则v(SO3)=0.35 mol/(L·min)
C.若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)<1.4 mol
D.若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量大于
Q kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学研究性学习小组对溶液作如下的归纳总结(均在常温下)。其中正确的是( )
①pH=3的强酸溶液1 mL,加水稀释至100 mL后,溶液pH降低2个单位
②1 L 0.50 mol·L-1 NH4Cl 溶液与2 L 0.25 mol·L-1 NH4Cl 溶液含NH4+ 物质的量前者大
③在某钠盐溶液中含有等物质的量的Cl-、I-、AlO2-、CO32-、NO3-、SiO32-中若干种,当加入过量的盐酸产生气泡,溶液颜色变深,阴离子种数减少3种,则原溶液中一定有CO32-
④pH=4、浓度均为0.1 mol·L-1 的CH3COOH、CH3COONa混合溶液中:
c(CH3COO-)-c(CH3COOH)=2×(10-4-10-10) mol/L
A.①② B.②③ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
聚乙酸乙烯酯广泛用于制备涂料、粘合剂等,它和高聚物长的合成路线如下;,
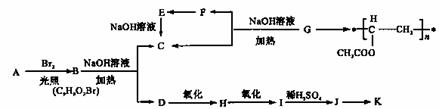
其中J物质与氯化铁溶液能发生显色反应,且苯环上的一元取代物有两种。
已知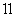 当羟基与双键碳原子相连时,易发生如下转化RCH =CHOH→RCH2CHO
当羟基与双键碳原子相连时,易发生如下转化RCH =CHOH→RCH2CHO
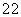 一ONa连在烃基生不会被氧化
一ONa连在烃基生不会被氧化
请回答下列问题:
(1)写出G的结构简式 。F与H中具有相同官能团的名称 。
(2)上述变化中G→C+F 的反应类型是 ;J在-定条件下能生成高聚物K,K的结构简式是
(3)写出B→C+D反应的化学方程式: 。
(4)同时符合下列要求的A的同分异构体有 种。
I含有苯环 II能发生银镜反应和水解反应
并写出满足下列条件的同分异构体结构简式: 。
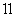 核磁共振氢谱有5 个吸收峰;
核磁共振氢谱有5 个吸收峰;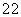 1mol该同分异构体能与Imol NaOH 反应
1mol该同分异构体能与Imol NaOH 反应
(5)下列有关说法正确的是 。
A.1 mol A 完全燃烧消耗10.5 mol O2
b.J与足量的碳酸氢钠溶液反应能生成相应的二钠盐·
c.D→H 的试剂通常是KMO4 酸性溶液
d.J能发生加成、消去、取代、氧化等反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组用0.50 mol·L- 1 NaOH溶液和0.50mol·L- 1 。1硫酸溶液进行中和热的测定。
Ⅰ.配制0.50mol·L- 1 硫酸溶液
(1)若配制250 mL硫酸溶液,则须用量筒量取密度为1.84 g·cm- 3、质量分数为
98%的浓硫酸 mL。
Ⅱ.测定稀硫酸和稀氢氧化钠溶液中和热的实验装置如右图所示:
(2)仪器A的名称为 ;
(3)装置中碎泡沫塑料的作用是 ;

(4)写出该反应中和热的热化学方程式:(中和热为57.3 kJ·mol- 1)
;
(5)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①下表中的温度差平均值为 ℃;
②近似认为0.50mol·L- 1 NaOH溶液和0.50mol·L- 1 硫酸溶液的密度都是1g·cm- 3 ,中和后生成溶液的比热容c= 4.18 J·(g·℃)- 1 。则中和热△H= (取小数点后一位)。

③上述实验数值结果与57.3 kJ·mol- 1 有偏差,产生此实验偏差的原因可能是(填字母) 。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.一次性把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
.用某种酸处理高岭石时,会得到一种沉淀,该沉淀由X、Y、Z、W四种短周期元素组成,它的化学式为XYZW6,其中X、Y、Z位于同一周期且最外层电子数依次增大,Y2+与W-具有相同电子层结构,下列说法正确的是
A. 离子半径:Y2+>W- B. 原子半径:X>Y>Z>W
C. 单质沸点:X>Y>Z>W D.四种元素的简单离子均能破坏水的电离平衡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com