
分析 (1)根据催化剂能加快化学反应速率以及催化加快反应速率的原因;
(2)依据高锰酸钾溶液是强氧化剂具有腐蚀氧化橡胶管的小猪猪,选择酸式滴定管,依据四次消耗溶液体积可知选择25ml酸式滴定管可以完成实验要求;
(3)根据C(待测)═$\frac{c(标准)V(标准)}{V(待测)}$分析误差;
(4)分析反应过程和实验数据计算过氧化氢的质量分数.
解答 解:(1)开始滴入KMnO4溶液时反应速率很慢,随着KMnO4溶液滴入反应速率显著加快,最可能是反应生成了催化剂MnSO4,催化剂降低了反应所需的活化能,加快反应速率,
故答案为:反应中生成的 Mn2+具有催化作用;
(2)KMnO4溶液具有强氧化性,可以腐蚀橡皮管,故KMnO4溶液应装在酸式滴定管中,四次消耗KMnO4溶液的体积分别为20.00mL、19.98mL、20.02mL、22.00mL,所以选用25ml酸式滴定管可以完成实验,
故答案为:C;
(3)A、锥形瓶用待测液润洗,消耗标准液体积增大,根据C(待测)═$\frac{c(标准)V(标准)}{V(待测)}$分析,可知C(标准)增大,测定待测液浓度偏高,故A正确;
B、量取 H2O2溶液的滴定管用蒸馏水洗净,未用H2O2溶液润洗,浓度减小,消耗标准液体积减小,根据C(待测)═$\frac{c(标准)V(标准)}{V(待测)}$分析,可知C(标准)减小,测定结果偏低,故B错误;
C.滴定速度过快,又未摇匀,停止滴定后发现紫红色褪去,滴入的标准液减小,根据C(待测)═$\frac{c(标准)V(标准)}{V(待测)}$分析,可知C(标准)减小,测定结果偏低,故c错误;
D、滴定前读数时平视,滴定终点读数时仰视,滴定后观察滴定管读数时,视线低于刻度线,造成V(标准)偏大,根据C(待测)═$\frac{c(标准)V(标准)}{V(待测)}$,可知C(标准)偏大,故D正确;
故答案为:AD;
(4)过氧化氢溶液中过氧化氢质量=5.0ml×1.0g/ml=5g,用0.1000mol/L KMnO4溶液滴定,用同样方法滴定,四次消耗KMnO4溶液的体积分别为20.00mL、19.98mL、20.02mL、22.00ml,第四次误差较大舍去,平均 消耗高锰酸钾溶液体积=$\frac{20.00+19.98+20.02}{3}$=20mL;
根据反应 2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑
2 5
0.1000mol/L×0.0200L n(H2O2)
$\frac{2}{0.1000mol/L×0.0200L}$=$\frac{5}{n(H{\;}_{2}O{\;}_{2})}$,所以n(H2O2)=0.005mol,
则过氧化氢质量分数=$\frac{0.05mol×34g/mol}{5g}$×100%=3.40%,
故答案为:3.40%.
点评 本题考查了物质组成和性质的实验设计验证和分析判断,滴定实验过程的计算应用误差分析方法,掌握基础是关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | 只有① | C. | ②③ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 和
和 E、CH3CH2CH2CH3和
E、CH3CH2CH2CH3和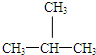
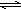 HCO3-+OH-
HCO3-+OH- 的系统命名为:3-甲基-4-乙基-庚烷
的系统命名为:3-甲基-4-乙基-庚烷 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com