
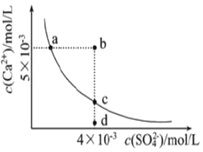
| A. | a、c两点均可以表示常温下CaSO4溶于水所形成的饱和溶液 | |
| B. | a点对应的Ksp不等于c点对应的Ksp | |
| C. | b点将有沉淀生成,平衡后溶液中c(Ca2+)•c(SO42-)一定等于9×10-6 | |
| D. | 向d点溶液中加入适量CaCl2固体可以变成c点 |
分析 A.曲线上的点为溶解平衡点;
B.Ksp只与温度有关;
C.b点Qc>Ksp;
D.向d点溶液中加入适量CaCl2固体,c(Ca2+)增大.
解答 解:A.曲线上的点为溶解平衡点,则a、c两点均可以表示常温下CaSO4溶于水所形成的饱和溶液,故A正确;
B.Ksp只与温度有关,a点对应的Ksp等于c点对应的Ksp,故B错误;
C.b点Qc>Ksp生成沉淀,平衡后溶液中c(Ca2+)•c(SO42-)一定等于9×10-6,故C正确;
D.向d点溶液中加入适量CaCl2固体,c(Ca2+)增大,则可以变成c点,故D正确;
故选B.
点评 本题考查难溶电解质的溶解平衡,为高频考点,把握图中平衡点、平衡移动、Ksp为解答的关键,侧重分析与应用能力的考查,注意Ksp只与温度有关,题目难度不大.


科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学试卷(解析版) 题型:选择题
下列做法不利于环境保护的是( )
A.开发太阳能、水能、风能、地热能等新能源
B.大力开采煤、石油和天然气,以满足人们日益增长的能源需求
C.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
D.减少资源消耗,注重资源的重复使用、资源的循环再生
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a<c+d | B. | A的转化率增大 | ||
| C. | D的体积分数变大 | D. | 平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;氯离子的电子式
;氯离子的电子式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
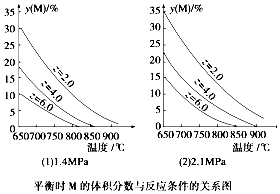
| A. | a+b<c+d | |
| B. | 同温同压时,增加z,平衡时Q的体积分数增加 | |
| C. | 同压同z时,升高温度,气体平均摩尔质量增加 | |
| D. | 同温同z时,增加压强,平衡时Q的物质的量浓度减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液和胶体的本质区别为是否能产生丁达尔效应 | |
| B. | K2Cr2O7溶液和氢溴酸能存放于同一药品橱内 | |
| C. | 用带玻璃塞的细口试剂瓶保存氢氟酸 | |
| D. | CH4和C2H4均属于常用危险品中的易燃气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
| c(N2O5)/(mol•L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
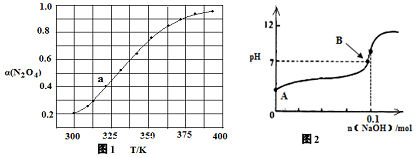
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com