
| A£® | ·ŹŌķĖ®”¢ĒāŃõ»ÆĢś½ŗĢå¾łŹōÓŚ½ŗĢå | |
| B£® | ½ŗĢåĒų·ÖÓŚĘäĖū·ÖÉ¢ĻµµÄ±¾ÖŹĢŲÕ÷ŹĒ·ÖÉ¢ÖŹĮ£×ÓÖ±¾¶“óŠ”ŌŚ1-100nmÖ®¼ä | |
| C£® | ÓĆĘ½ŠŠ¹āÕÕÉäNaClČÜŅŗŗĶFe£ØOH£©3½ŗĢåŹ±£¬²śÉśĻÖĻóĻąĶ¬ | |
| D£® | Fe£ØOH£©3½ŗĢåÄܹ»Ź¹Ė®ÖŠŠüø”ĪļµÄ¹ĢĢåæÅĮ£³Į½µ£¬“ļµ½¾»Ė®µÄÄæµÄ |
·ÖĪö A”¢øł¾Ż·ŹŌķĖ®Ņ²ŹĒ½ŗĢ壻
B”¢øł¾Ż½ŗĢåĒų±šÓŚĘäĖū·ÖÉ¢ĻµµÄ±¾ÖŹĢŲÕ÷ŹĒ·ÖÉ¢ÖŹµÄĪ¢Į£Ö±¾¶“󊔣»
C”¢øł¾ŻČÜŅŗ²»¾ßÓŠ¶”“ļ¶ūŠ§Ó¦£¬¶ų½ŗĢå¾ßÓŠ¶”“ļ¶ūŠ§Ó¦£¬
D”¢øł¾ŻFe£ØOH£©3 ½ŗĢåµÄ±ķĆ껿½Ļ“ó£¬ÄÜĪüø½Ė®ÖŠŠüø”µÄ¹ĢĢåæÅĮ£“ļµ½¾»Ė®µÄÄæµÄ£®
½ā“š ½ā£ŗA”¢·ŹŌķĖ®”¢ĒāŃõ»ÆĢś½ŗĢå¾łŹōÓŚ½ŗĢ壬¹ŹAÕżČ·£»
B”¢½ŗĢåĒų±šÓŚĘäĖū·ÖÉ¢ĻµµÄ±¾ÖŹĢŲÕ÷ŹĒ·ÖÉ¢ÖŹµÄĪ¢Į£Ö±¾¶“󊔣¬½ŗĢå·ÖÉ¢ĻµµÄĪ¢Į£Ö±¾¶ŌŚ1”«100nmÖ®¼ä£¬¹ŹBÕżČ·
C”¢NaClČÜŅŗ²»¾ßÓŠ¶”“ļ¶ūŠ§Ó¦£¬¶ųFe£ØOH£©3½ŗĢå¾ßÓŠ¶”“ļ¶ūŠ§Ó¦£¬ĻÖĻó²»ĻąĶ¬£¬¹ŹC“ķĪó£»
D”¢Fe£ØOH£©3 ½ŗĢåµÄ±ķĆ껿½Ļ“ó£¬ÄÜĪüø½Ė®ÖŠŠüø”µÄ¹ĢĢåæÅĮ£“ļµ½¾»Ė®µÄÄæµÄ£¬¹ŹDÕżČ·£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éѧɜ½ŗĢåµÄĢŲŠŌŅŌ¼°ČÜŅŗŗĶ½ŗĢåµÄ±¾ÖŹĒų±š£¬ĢāÄæÄŃ¶Č²»“ó£¬ŹģĻ¤½ŗĢåµÄŠŌÖŹŹĒ½ā“šµÄ¹Ų¼ü£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | £ØNH4£©2SO4ČÜŅŗÖŠ£ŗc£ØSO42-£©£¾c£ØNH4+£©£¾c£ØH+£©£¾c£ØOH-£© | |
| B£® | NaHCO3ČÜŅŗÖŠ£ŗc£ØNa+£©=c£ØHCO3-£©+c£ØH2CO3£©+2c£ØCO32-£© | |
| C£® | °±Ė®ÖŠ£¬c£ØOH-£©=c£ØNH4+£© | |
| D£® | NH4ClČÜŅŗÖŠ£ŗc£ØCl-£©=c£ØNH4+£©+c£ØNH3•H2O£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | µć¢ŁŹ±£ŗc£ØCN-£©£¾c£ØNa+£©£¾c£ØHCN£©£¾c£ØOH-£© | |
| B£® | µć¢ŪŹ±£ŗc£ØNa+£©=c£ØCH3COO-£©£¾c£ØH+£© | |
| C£® | µć¢ÜŹ±£ŗc£ØNa+£©£¾c£ØCH3COO-£©£¾c£ØOH-£©£¾c£ØH+£© | |
| D£® | µć¢ŁŗĶµć¢ŚĖłŹ¾ČÜŅŗÖŠ£ŗc£ØCH3COO-£©-c£ØCN-£©=c£ØHCN£©-c£ØCH3COOH£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
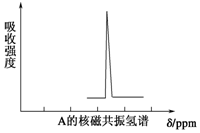 ÓŠŅ»ÖÖŠĀŗĻ³ÉµÄø߶ȶŌ³ĘµÄÓŠ»śĪļA£®ŅŃÖŖ10.4g AŌŚ×ćĮæO2ÖŠ³ä·ÖČ¼ÉÕ£¬½«Éś³ÉµÄ»ģŗĻĘųĢåŅĄ“ĪĶعż×ćĮæµÄÅØĮņĖįŗĶ¼īŹÆ»Ņ£¬·Ö±šŌöÖŲ7.2gŗĶ35.2g£¬¾¼ģŃéŹ£ÓąĘųĢåĪŖO2£®
ÓŠŅ»ÖÖŠĀŗĻ³ÉµÄø߶ȶŌ³ĘµÄÓŠ»śĪļA£®ŅŃÖŖ10.4g AŌŚ×ćĮæO2ÖŠ³ä·ÖČ¼ÉÕ£¬½«Éś³ÉµÄ»ģŗĻĘųĢåŅĄ“ĪĶعż×ćĮæµÄÅØĮņĖįŗĶ¼īŹÆ»Ņ£¬·Ö±šŌöÖŲ7.2gŗĶ35.2g£¬¾¼ģŃéŹ£ÓąĘųĢåĪŖO2£®
 £¬ĘäŗĖ“Ź²ÕńĒāĘ×ÓŠ5øöĪüŹÕ·å£®
£¬ĘäŗĖ“Ź²ÕńĒāĘ×ÓŠ5øöĪüŹÕ·å£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ąė×Ó | SO42- | SO32- | NO3- | NO2- | Cl- |
| c/£Ømol•L-1£© | 8.35”Į10-4 | 6.87”Į10-6 | 1.5”Į10-4 | 1.2”Į10-5 | 3.4”Į10-3 |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 »Ų“šĻĀĮŠĪŹĢā£ŗ
»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹµŃé²Ł×÷ | ŹµŃéĻÖĻó | ½įĀŪ |
| A | ½«ĮņµÄ¾Ę¾«ČÜŅŗµĪČėŅ»¶ØĮæµÄČČĖ®ÖŠµĆĪ¢Ą¶É«ĶøĆ÷ŅŗĢ壬ÓĆ¼¤¹ā±ŹÕÕÉä | ÓŠ¶”“ļ¶ūŠ§Ó¦ | Ī¢Ą¶É«ĶøĆ÷ŅŗĢåĪŖ½ŗĢå |
| B | ½«FeSO4øßĪĀĒæČČ£¬µĆŗģÉ«¹ĢĢ壬²śÉśµÄĘųĢåĶØČėBaCl2ČÜŅŗ | ²śÉś°×É«³Įµķ | °×É«³ĮµķĪŖBaSO4ŗĶBaSO3 |
| C | Č”½«ĘųĢåX·Ö±šĶØČėĘ·ŗģČÜŅŗŗĶĖįŠŌøßĆĢĖį¼ŲČÜŅŗ | Į½ČÜŅŗ¾łĶŹÉ« | XæÉÄÜŹĒŅŅĻ© |
| D | ĻņČÜŅŗYÖŠµĪ¼ÓĻõĖį£¬ŌŁµĪ¼ÓBaCl2ČÜŅŗ | ÓŠ°×É«³Įµķ | YÖŠŅ»¶Øŗ¬ÓŠSO42- |
| A£® | A”¢ | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 Ņ»¶ØĢõ¼žĻĀ£¬Ä³ČŻĘ÷ÖŠø÷Ī¢Į£ŌŚ·“Ó¦Ē°ŗó±ä»ÆµÄŹ¾ŅāĶ¼ČēĻĀ£¬ĘäÖŠ”ńŗĶ”š“ś±ķ²»Ķ¬ŌŖĖŲµÄŌ×Ó£®¹ŲÓŚ“Ė·“Ó¦Ėµ·Ø“ķĪóµÄŹĒ£Ø””””£©
Ņ»¶ØĢõ¼žĻĀ£¬Ä³ČŻĘ÷ÖŠø÷Ī¢Į£ŌŚ·“Ó¦Ē°ŗó±ä»ÆµÄŹ¾ŅāĶ¼ČēĻĀ£¬ĘäÖŠ”ńŗĶ”š“ś±ķ²»Ķ¬ŌŖĖŲµÄŌ×Ó£®¹ŲÓŚ“Ė·“Ó¦Ėµ·Ø“ķĪóµÄŹĒ£Ø””””£©| A£® | Ņ»¶ØŹōÓŚæÉÄę·“Ó¦ | B£® | Ņ»¶ØŹōÓŚ·ÅČČ·“Ó¦ | ||
| C£® | Ņ»¶ØŹōÓŚŃõ»Æ»¹Ō·“Ó¦ | D£® | Ņ»¶ØŹōÓŚ·Ö½ā·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com