
 CH3COCH2COH(CH3)2(l)�� ȡ����CH3COCH3���ֱ���0���20���£������ת��������ʱ��仯�Ĺ�ϵ���ߣ�Y��t������ͼ��ʾ������˵����ȷ����
CH3COCH2COH(CH3)2(l)�� ȡ����CH3COCH3���ֱ���0���20���£������ת��������ʱ��仯�Ĺ�ϵ���ߣ�Y��t������ͼ��ʾ������˵����ȷ����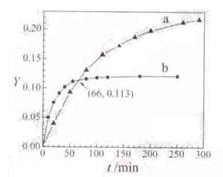
| A��b����0����CH3COCH3��Y��t���� |
B����Ӧ���е�20minĩ��H3COCH3��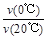 >1 >1 |
| C�������¶ȿ����̷�Ӧ��ƽ���ʱ�䲢�����ƽ��ת���� |
D����Y=0��Y=0.113��CH3COCH2COH(CH3)2��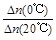 =1 =1 |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
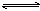 2C(g)��D(g),����aΪ����������Ӧ�����У���������������ʱ��C�İٷֺ�����C�������¶ȣ�T����ѹǿ��P���Ĺ�ϵ��ͼ,����������ȷ����
2C(g)��D(g),����aΪ����������Ӧ�����У���������������ʱ��C�İٷֺ�����C�������¶ȣ�T����ѹǿ��P���Ĺ�ϵ��ͼ,����������ȷ����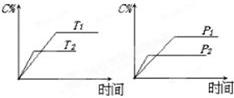
| A���ﵽƽ����������C������ |
| B���ﵽƽ����������¶ȣ�ƽ�������ƶ� |
| C��a��������������� |
| D����ƽ�������A������������ƽ�������ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
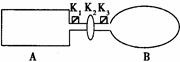
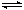 N2O4����H<0������������϶�ƽ���ƶ���Ӱ�� )
N2O4����H<0������������϶�ƽ���ƶ���Ӱ�� ) �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��2NO2��g�� N2O4��g�� ��H��0 N2O4��g�� ��H��0 |
B��3O2��g�� 2O3��g����H��0 2O3��g����H��0 |
C��H2��g��+I2��g�� 2HI��g����H��0 2HI��g����H��0 |
D��NH4HCO3��s�� NH3��g��+H2O��g��+CO2��g�� ��H��0 NH3��g��+H2O��g��+CO2��g�� ��H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 SO3(g)����H����98.3 kJ��mol��1
SO3(g)����H����98.3 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
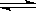 CO(g)+H2(g)����ƽ�ⳣ������ʽ��ȷ���ǣ� ��
CO(g)+H2(g)����ƽ�ⳣ������ʽ��ȷ���ǣ� ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 xC(g)+2D(g)��2minĩ��Ӧ�ﵽƽ��״̬��������0.8molD�������C��Ũ��Ϊ0.4mol/L������д���пհף�
xC(g)+2D(g)��2minĩ��Ӧ�ﵽƽ��״̬��������0.8molD�������C��Ũ��Ϊ0.4mol/L������д���пհף�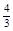 mol��Ҫʹƽ��ʱ�����ʵ�����������ԭƽ��ʱ��ȫ��ȣ���Ӧ����________����_________mol
mol��Ҫʹƽ��ʱ�����ʵ�����������ԭƽ��ʱ��ȫ��ȣ���Ӧ����________����_________mol�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 C(g)+D(g) ��֪��ƽ��ʱ��Ca(A)��C(B)= C(C)��C(D),Ȼ�����¶Ȳ��������£����������ݻ���ԭ��10�������A�İٷֺ���ʼ��δ�иı䣬��B��ת������ �� ��
C(g)+D(g) ��֪��ƽ��ʱ��Ca(A)��C(B)= C(C)��C(D),Ȼ�����¶Ȳ��������£����������ݻ���ԭ��10�������A�İٷֺ���ʼ��δ�иı䣬��B��ת������ �� ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com