
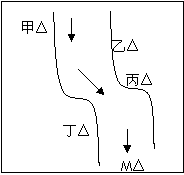
 ��һ���㡢Ϻ������С�ӱ��������������ס��ҡ�����������ͼ��ʾ���������ų��ķ�Һ�ÿ������ֻ����Na2CO3��FeCl3��Ca(OH)2��HCl�е�һ�֡�ij��ѧ����С��Ժ�ˮ���ʱ���֣��ټ״���ˮ�����ɫ�����Ҵ���ˮ�ʺ��ɫ���۱�����ˮ�ɻ���壬�ܶ����������ݣ���ˮ���壬��M��ˮ����pHС��7�����жϣ�
��һ���㡢Ϻ������С�ӱ��������������ס��ҡ�����������ͼ��ʾ���������ų��ķ�Һ�ÿ������ֻ����Na2CO3��FeCl3��Ca(OH)2��HCl�е�һ�֡�ij��ѧ����С��Ժ�ˮ���ʱ���֣��ټ״���ˮ�����ɫ�����Ҵ���ˮ�ʺ��ɫ���۱�����ˮ�ɻ���壬�ܶ����������ݣ���ˮ���壬��M��ˮ����pHС��7�����жϣ�
��1�����������ų��ķ�Һ�ﺬ�е���Ⱦ�
�� �� �� ��
�� ���� ��
��2����M��ȡ���ĺ�ˮ�У��϶����е�������
��
��3��д�� �� ���������ӷ�Ӧ
�� ���������ӷ�Ӧ
 ��У���˳�̾�ϵ�д�
��У���˳�̾�ϵ�д� ��У���һ��ͨϵ�д�
��У���һ��ͨϵ�д� �γ̴����Ծ�����100��ϵ�д�
�γ̴����Ծ�����100��ϵ�д� �¾�����ĩ���100��ϵ�д�
�¾�����ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и�����������Hԭ��������(����)
A��0.1 mol NH4Cl
B��0.1 mol NH4HCO3
C��0.2 mol H2
D��0.2 mol H3PO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ʵ��������������ԭ�����͵��ǣ� ��
A������ɫNO2��ѹ����ɫ�ȱ�����dz
B��ʵ�����г����ű���ʳ��ˮ�ķ����ռ�������
C��SO2��������SO3�ķ�Ӧ��ʹ�ù����Ŀ�������߶��������������
D��ѹ��H2��I2��g����Ӧ��ƽ�������壬��ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��2.0mol/LCuSO4��Һ��1.0mol/LH2SO4��Һ�������ϣ������Ϻ���Һ�������������Һ�����֮�ͣ���������Һ�м������������ۣ����㹻����ʱ���������ʣ�ࡣ��ʱ����Һ�е�Fe2+���ʵ���Ũ��Ϊ �� ��
A 0.5 mol/L B 1.5 mol/L C 1.0 mol/L D 2mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и����������������Һ�еķ�Ӧ,����ͬһ���ӷ���ʽ��ʾ����
A��Cu(OH)2������,Cu(OH)2�����
B��BaCl2��Һ��Na2SO4��Һ,Ba(OH)2��Һ��H2SO4��Һ
C��NaHCO3��Һ������,Na2CO3��Һ������
D��ʯ��ʯ�����ᷴӦ,ʯ��ʯ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ij�л��� 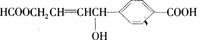 ������������ȷ���� ��������
������������ȷ���� ��������
A��1 mol���л��������3 mol Na������Ӧ��
B��1 mol���л��������3 mol NaOH������Ӧ
C��1 mol���л��������6 mol H2�����ӳɷ�Ӧ
D��1 mol���л���ֱ�������Na��NaHCO3��Ӧ����������������ͬ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ײ��϶�������(TiO2)���кܸߵĻ�ѧ���ԣ��������������Ĵ�����
��1����ҵ�϶������ѵ��Ʊ��ǣ�
I. �������Ľ��ʯ(��Ҫ�ɷ�TiO2,��Ҫ����SiO2)��̼�ۻ��װ���Ȼ�¯�У��ڸ�����ͨ��Cl2,�Ƶû���SiCl4���ʵ�TiCl4��
II. ������SiCl4���ʵ�TiCl4���룬�õ�������TiCl4��
III. ��TiCl4�м�ˮ�����ȣ�ˮ��õ�����TiO2•xH2O��
IV. TiO2��xH2O���·ֽ�õ�TiO2��
��TiCl4��SiCl4�ڳ����µ�״̬��_______��II������ȡ�IJ�������_______��
|
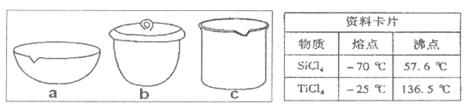
����ʵ��IV�У�Ӧ��TiO2.xH2O����_______ (���������)�м��ȡ�
��2���ݱ���������̬��·����������ʱ����һ������TiO2,TiO2��̫������������ĵ��ӱ�������ˮ�е�����ã�����H2O2,����̴������£�
���� a. O2��2O b. O+H2O��2OH(�ǻ�) c. OH+OH��H2O2
��b���ƻ����ǡ���������������������Թ��ۼ����Ǽ��Թ��ۼ�������
��H2O2�����·������е�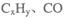 �ȣ�����Ҫ��������H2O2�ġ���������������ԡ���ԭ�ԡ�����
�ȣ�����Ҫ��������H2O2�ġ���������������ԡ���ԭ�ԡ�����
��3��������������Ҫ�Ļ�ѧ�Լ�������ˮ��Һ�ֳ�Ϊ˫��ˮ��������������ɱ����Ư�ȡ�ij��ѧ��ȤС��ȡһ�����Ĺ���������Һ��ȷ�ⶨ�˹�������ĺ�����
����д���пհף�
��ȡ10.00 mL�ܶ�ΪP g/mL�Ĺ���������Һϡ����250 mL��ȡϡ�ͺ�Ĺ���������Һ25.00mL����ƿ�У�����ϡ�����ữ��������ˮϡ�ͣ�������������
�ø�����ر���Һ�ζ������������䷴Ӧ�����ӷ���ʽ���£��뽫������ʵĻ�ѧ��������ƽ����ѧʽ��д�ڷ����
 MnO+ H2O2+ H+= Mn2++ H2O+
MnO+ H2O2+ H+= Mn2++ H2O+
�ڵζ�ʱ����������ر���Һע��______________�����ʽ����ʽ�����ζ����С��ζ������յ��������____________________________��
���ظ��ζ����Σ�ƽ������C mol/L KMnO4����Һ V mL,��ԭ����������Һ�й����������������Ϊ______________��
�����ζ�ǰ�ζ��ܼ����������ݣ��ζ���������ʧ����ⶨ���_________ ���ƫ�ߡ���ƫ�͡����䡱����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ�������£�pH��ͬ���������������Һ��ˮ���������c(H+)�ֱ���1.0��10-amol��L-1 ��1.0��10-bmol��L-1���ڴ��¶��£�����˵����ȷ��
A��a<b B��a=b
C��ˮ�����ӻ�Ϊ1.0��10-(7+a) D��ˮ�����ӻ�Ϊ1.0��10-(b+a)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ʵ�������0.1 mol��CH3COOH��CH3COONa���Ƴ�1L�����Һ����֪����C(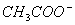 )��C(Na+)���Ըû����Һ�������ж���ȷ����( )
)��C(Na+)���Ըû����Һ�������ж���ȷ����( )
����A.C(H+)��C(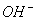 ) B.C(CH3COOH)��C(
) B.C(CH3COOH)��C(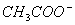 )��0.2 mol/L
)��0.2 mol/L
����C.C(CH3COOH)��C(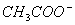 ) D.C(CH3COO-)��C(
) D.C(CH3COO-)��C(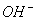 )��0.2 mol/L
)��0.2 mol/L
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com