��2012?ʯ��ɽ��һģ��������ȼ��ʱ�ܷų��������ȣ���Ҳ��Һ��ʯ��������Ҫ�ɷ֣���Ϊ��ԴӦ�������ǵ��ճ����������
��֪����2C
3H
8��g��+7O
2��g���T6CO��g��+8H
2O ��l����H
1=-2741.8kJ/mol
��2CO ��g��+O
2��g���T2CO
2��g����H
2=-566kJ/mol
��1����ӦC
3H
8��g��+5O
2��g���T3CO
2��g��+4H
2O ��l�� �ġ�H=
-2219.9kJ/mol
-2219.9kJ/mol
��
��2������1mol C
3H
8�ڲ�������������ȼ�գ�����1mol CO��2mol CO
2�Լ���̬ˮ�������еIJ���ͨ��һ���̶����Ϊ1L���ܱ������У���һ�������·������¿��淴Ӧ��CO��g��+H
2O ��g��?CO
2��g��+H
2��g����H=+41.2kJ/mol
��������ʵ��˵���÷�Ӧ�ﵽƽ�����
d
d
��
a����ϵ�е�ѹǿ�������仯
b��v
����H
2��=v
����CO��
c����������ƽ����Է��������������仯
d��CO
2��Ũ�Ȳ��ٷ����仯
��5min����ϵ�ﵽƽ�⣬���ⶨ��H
2Ϊ0.8mol����v��H
2��=
0.16mol/��L?min��
0.16mol/��L?min��
��
����ƽ����ϵ�г�������CO��ƽ�ⳣ��
����
����
�����������С�����䡱����
��3�����ݣ�1���еķ�Ӧ�������һ������ȼ�ϵ�أ�һ��ͨ���������һ��ͨ��������壻ȼ�ϵ���ڲ������ڵIJ����������ƣ�Y
2O
3��������ﯣ�ZrO
2�����壬�����ڲ����Դ���O
2-���ڵ���ڲ�O
2-��
��
��
������
��
��
�������������������صĸ����缫��ӦʽΪ
C3H8+10O2--20e-=3CO2+4H2O
C3H8+10O2--20e-=3CO2+4H2O
��
��4��������ȼ�ϵ�غͶ��Ե缫�������Mg��NO
3��
2��NaCl�Ļ����Һ����ʼ������������Ϊ
����ɫ�������ɣ��а�ɫ��������
����ɫ�������ɣ��а�ɫ��������
��

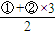 �ɵ�C3H8��g��+5O2 ��g��=3CO2 ��g��+4H2O��
�ɵ�C3H8��g��+5O2 ��g��=3CO2 ��g��+4H2O��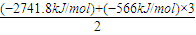 =-2219.9KJ/mol��
=-2219.9KJ/mol��

