
 ③CH3CH2Br④
③CH3CH2Br④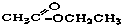 ⑤
⑤ ⑥
⑥
 ⑧
⑧ ⑨
⑨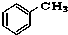 ⑩
⑩
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫能使酸性高锰酸钾溶液褪色 | |
| B. | 氯水能使甲基橙褪色 | |
| C. | 浓硝酸能使石蕊试液褪色 | |
| D. | 臭氧能使品红溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核素是指质量数相同的微粒 | |
| B. | 核素是指 质子数相同、中子数不同的微粒 | |
| C. | 核素是指具有一定数目的质子和一定数目的中子的一种原子 | |
| D. | 核素是指质子数相同、核外电子数不同的微粒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油是混合物,汽油是纯净物 | |
| B. | 分馏汽油和裂解汽油成分相同 | |
| C. | 沸点:汽油>煤油>柴油>润滑油 | |
| D. | 石油的分馏是物理过程,而裂化合裂解是化学过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在离子化合物中,可能含共价键 | |
| B. | 在共价化合物中,可能含离子键 | |
| C. | 含共价键的化合物一定是共价化合物 | |
| D. | 含离子键的化合物不一定是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正反应生成的NH3速率和逆反应生成N2的速率相等 | |
| B. | 反应器中压强不随时间变化而变化 | |
| C. | 1molN≡N键断裂的同时,有6molN-H键断裂 | |
| D. | 混合气体平均分子量保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硫代硫酸钠(Na2S2O3•5H2O)是一种脱氯剂,它易溶于水,难溶于乙醇,40~45℃熔化,48℃分解,由硫化钠和亚硫酸钠制备,涉及的反应原理为:
硫代硫酸钠(Na2S2O3•5H2O)是一种脱氯剂,它易溶于水,难溶于乙醇,40~45℃熔化,48℃分解,由硫化钠和亚硫酸钠制备,涉及的反应原理为: .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com