
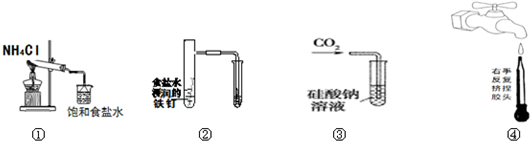
| A. | 实验①制取的氨气溶解在饱和NaCl溶液 | |
| B. | 实验②通过观察右边试管有无倒吸现象说明铁钉是否发生吸氧腐蚀 | |
| C. | 实验③可用于证明碳的非金属性比硅强 | |
| D. | 图④是实验室洗涤胶头滴管的操作 |
分析 A.加热氯化铵生成氨气与氯化氢,氯化氢与氨气遇冷又生成氯化铵,无法获得氨气;
B.试管口没盖塞子;
C.利用强酸制备弱酸,酸性越强,最高价氧化物水化物的酸性越强,中心元素的非金属性越强;
D.药品进入胶头,会腐蚀胶头.
解答 解:A.氯化铵分解无法获得氨气,实验室用氢氧化钙和氯化铵制取氨气,故A错误;
B.试管口没盖塞子,看不到倒吸,故B错误;
C.利用强酸制备弱酸,酸性越强,最高价氧化物水化物的酸性越强,中心元素的非金属性越强,二氧化碳和水反应生成碳酸,碳酸和可溶性硅酸盐反应析出硅酸白色沉淀,说明碳酸能制取硅酸,盛有Na2SiO3溶液的试管中出现白色沉淀,说明碳的非金属性比硅强,故C正确;
D.药品进入胶头,会腐蚀胶头,不能倒立,故D错误.
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及物质制备、金属腐蚀、非金属性比较以及实验操作等,把握实验技能及化学反应原理为解答的关键,侧重分析与实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:H2SO4>H3PO4 | B. | 非金属性:O>S | ||
| C. | 碱性:NaOH>Mg(OH)2 | D. | 沸点:HF>HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氨在国民经济中占有很重要的地位.现在约有80%的氨用来制造化肥,其余的用作生产其他化工产品的原料.氨氧化法制硝酸是工业上制硝酸的主要方法.
氨在国民经济中占有很重要的地位.现在约有80%的氨用来制造化肥,其余的用作生产其他化工产品的原料.氨氧化法制硝酸是工业上制硝酸的主要方法.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂发生皂化反应能生成甘油 | |
| B. | 蔗糖水解前后均可发生银镜反应 | |
| C. | Fe、Cu、Ag三种金属常用化学还原剂还原法制得 | |
| D. | 向蛋白质溶液中加入CuSO4溶液发生盐析 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(S2-)+c(HS-)+c(H2S)+c(H+)=c(OH-) | B. | c(OH-)=c(HS-)+c(H+)+2 c(H2S) | ||
| C. | c(Na+)=c(S2-)+c(HS-)+c(H2S) | D. | c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该物质属于烃类 | B. | 该物质易溶于水 | ||
| C. | 该物质能使酸性高锰酸钾溶液褪色 | D. | 该物质是一种高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 25℃,1.01×105 Pa,64g SO2中含有的原子数为3NA | |
| B. | 在1mol的Na2O2晶体中离子总数为3NA | |
| C. | 在0.5mol/L NaCl溶液中,含有的Na+数目为0.5NA | |
| D. | 标准状况下,11.2LH2O 含有的分子数为0.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com