
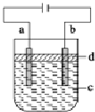
| A. | a电极的材料应为铁 | |
| B. | d为苯,其作用为防止空气中的O2把Fe(OH)2氧化 | |
| C. | 电解液c可以是NaCl溶液、NaOH溶液等 | |
| D. | 若电解过程中阳极消耗铁11.2g,理论上阴极产生气体为4.48L |
分析 A.因为Fe(OH)2极易被氧化,为防止Fe(OH)2被氧化,用电解原理制取Fe(OH)2,应该用Fe作阳极、石墨作阴极;
B.Fe(OH)2极易被氧化,所以制取Fe(OH)2时要隔绝空气;
C.阳极上生成的Fe 2+和阴极生成的OH-或溶液中OH-反应生成Fe(OH)2;
D.气体摩尔体积与温度、压强有关,温度和压强未知导致气体摩尔体积未知.
解答 解:A.因为Fe(OH)2极易被氧化,为防止Fe(OH)2被氧化,用电解原理制取Fe(OH)2,应该用Fe作阳极、石墨作阴极,则Fe作a电极、石墨作b电极,故A正确;
B.Fe(OH)2极易被氧化,所以制取Fe(OH)2时要隔绝空气,苯和水不互溶且密度小于水,所以d为苯能隔绝空气,故B正确;
C.阳极上生成的Fe 2+和阴极生成的OH-或溶液中OH-反应生成Fe(OH)2,所以电解质溶液可以是NaCl溶液、NaOH溶液等,故C正确;
D.气体摩尔体积与温度、压强有关,温度和压强未知导致气体摩尔体积未知,则无法计算阴极生成气体体积,故D错误;
故选D.
点评 本题以Fe(OH)2的制备为载体考查电解原理,为高频考点,侧重考查学生获取信息并灵活运用信息解答问题能力,涉及气体摩尔体积适用条件、电极材料的判断等知识点,明确电解原理、物质性质及气体摩尔体积适用条件是解本题关键,易错选项是D.


科目:高中化学 来源: 题型:选择题
| A. | 沸点:H2O>H2S | B. | 碱性:KOH>NaOH | ||
| C. | 酸性:HClO4>H2SO4 | D. | 元素的金属性:Mg>Al |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
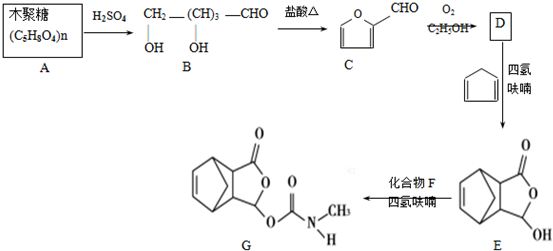
 ,在流程中作反应的催化剂;
,在流程中作反应的催化剂; ;
;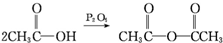 .
. 、CH3NHCOOH.
、CH3NHCOOH. .
. .
.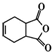 )是合成抗病毒药物阿昔洛韦的中间体.参照上述合成路线,写出以1,3-丁二烯为原料制备H的合成路线流程图(无机试剂任用):
)是合成抗病毒药物阿昔洛韦的中间体.参照上述合成路线,写出以1,3-丁二烯为原料制备H的合成路线流程图(无机试剂任用): .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
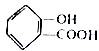
 与
与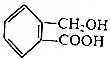 互为同系物
互为同系物 ,请写出将
,请写出将 转化为
转化为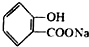 的化学方程式
的化学方程式 +NaHCO3→
+NaHCO3→ +H2O+CO2↑.
+H2O+CO2↑.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、I-、CO${\;}_{3}^{2-}$、ClO- | B. | Fe2+、H+、K+、NO${\;}_{3}^{-}$ | ||
| C. | Ba2+、Na+、SCN-、Cl- | D. | Cu2+、Fe2+、Cl-、NO${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.4 mol | B. | 0.6 mol | C. | 0.8 mol | D. | 1.0 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲一定是强碱 | B. | 乙一定是弱碱 | C. | 乙一定是二元碱 | D. | 甲一定是一元碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
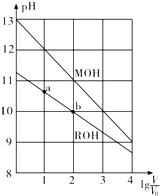
| A. | MOH的碱性强于ROH的碱性 | |
| B. | ROH的电离程度:b点大于a点 | |
| C. | 当1g$\frac{V}{{V}_{0}}$=2时,若两溶液同时升温,则$\frac{c({M}^{+})}{c({R}^{+})}$增大 | |
| D. | 若两溶液无限稀释,则它们的c(OH-)相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com