
| c(标)×V(标) |
| V(待) |
| c(标)×V(标) |
| V(待) |
| c(标)×V(标) |
| V(待) |


科目:高中化学 来源:不详 题型:单选题
| A.用焰色反应鉴别NaCl和Na2SO4 |
| B.用氢氧化钠溶液鉴别MgCl2溶液和AlCl3溶液 |
| C.利用丁达尔效应鉴别硅酸溶胶和NaCl溶液 |
| D.用品红试液鉴别SO2和CO2两种气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.一定有Na+,也可能有K+ | B.一定有Na+,也一定有K+ |
| C.可能有Na+,也可能有K+ | D.只有Na+ |
查看答案和解析>>
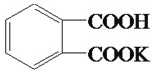
科目:高中化学 来源:不详 题型:问答题
| 实验编号 | 邻苯二甲酸氢钾的质量(g) | 待测NaOH溶液的体积(mL) |
| 1 | 0.4162 | 18.25 |
| 2 | 17.04 | |
| 3 | 16.96 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| V(HCl)/mL | 0.00 | 12.00 | 18.00 | 22.00 | 23.00 | 23.96 | 24.00 | 24.04 | 25.00 | 26.00 | 30.00 |
| pH | 13.1 | 12.6 | 12.2 | 11.7 | 11.4 | 9.9 | 7.0 | 4.0 | 2.7 | 2.4 | 1.9 |
| 指示剂 | 变色范围 (pH) | 各范围内颜色 | ||
| 前 | 中间 | 后 | ||
| 甲基橙 | 3.1~4.4 | 红 | 橙色 | 黄 |
| 石蕊 | 5.0~8.0 | 红 | 紫色 | 蓝 |
| 酚酞 | 8.2~10.0 | 无 | 粉红 | 红 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
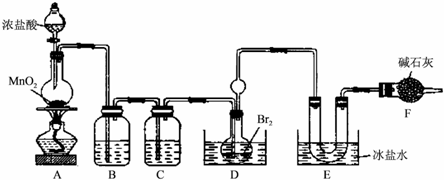
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH4Cl稀溶液、NaOH稀溶液、碱石灰 |
| B.饱和氨水、NaOH固体、五氧化二磷固体 |
| C.NaOH溶液、NH4Cl晶体、浓H2SO4 |
| D.NH4Cl固体、消石灰、碱石灰 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com