
聚合硫酸铁(PPS)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理.用铁的氧化物为原料来制取聚合硫酸铁,为控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+必须先还原成Fe2+.实验步骤如下:

(1)用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒外,还有________.
a.容量瓶 b.烧杯 c.烧瓶
(2)步骤Ⅱ取样分析溶液中的Fe2+、Fe3+的含量,目的是________.
a.控制溶液中Fe2+与Fe3+含量比
b.确定下一步还原所需铁的量
c.确定氧化Fe2+所需NaClO3的量
d.确保铁的氧化物酸溶完全
(3)聚合硫酸铁溶液中![]() 与Fe3+物质的量之比不是3∶2.根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中
与Fe3+物质的量之比不是3∶2.根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中![]() 与Fe3+物质的量之比.测定时所需的试剂为________,需要测定________和________的质量.(填写化合物的化学式)
与Fe3+物质的量之比.测定时所需的试剂为________,需要测定________和________的质量.(填写化合物的化学式)
a.NaOH b.FeSO4 c.BaCl2 d.NaClO3
|
答案:(1)b (2)bc (3)ac Fe2O3 BaSO4 解析:本题以合成聚合硫酸铁为载体,综合考查了实验基础知识:液体的稀释、沉淀的生成、过滤、洗涤、干燥等操作.浓硫酸的稀释应在烧杯中进行,且把浓硫酸注入水中;步骤Ⅱ取样分析溶液中的Fe2+、Fe3+的含量,目的是确定下一步还原所需铁的量及确定氧化Fe2+所需NaClO3的量;测定 |


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:

(1)用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒外,还有_____________。
A.容量瓶 b.烧杯 c.烧瓶
(2)步骤Ⅱ取样分析溶液中的Fe2+、Fe3+的含量,目的是_______________________________。
A.控制溶液中Fe2+与Fe3+含量比
b.确定下一步还原所需铁的量
c.确定氧化Fe2+所需NaClO3的量
d.确保铁的氧化物酸溶完全
(3)用NaClO3氧化时反应方程式如下:
6FeSO4+NaClO3+3H2SO4====3Fe2(SO4)3+NaCl+3H2O
若改用HNO3氧化,则反应方程式如下:
6FeSO4+2HNO3+3H2SO4====3Fe2(SO4)3+2NO↑+4H2O
已知1 mol HNO3价格0.16元、1 mol NaClO3价格0.45元,评价用HNO3代替NaClO3作氧化剂的利弊。利是_____________________________,弊是__________________________________。
聚合硫酸铁溶液中SO![]() 与Fe3+物质的量之比不是3∶2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中SO
与Fe3+物质的量之比不是3∶2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中SO![]() 与Fe3+物质的量之比。
与Fe3+物质的量之比。
(4)测定时所需的试剂有__________。
A.NaOH b.FeSO4
C.BaCl2 d.NaClO3
(5)需要测定__________和__________的质量(填写化合物的化学式)。
(6)选出测定过程中所需的基本操作__________(按操作先后顺序列出)。
A.萃取、分液 b.过滤、洗涤 c.蒸发、结晶 d.冷却、称量 e.烘干或灼烧
查看答案和解析>>
科目:高中化学 来源: 题型:

(1)用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒外,还有______________。
a.容量瓶 b.烧杯 c.烧瓶
(2)步骤Ⅱ取样分析溶液中的Fe2+、Fe3+的含量,目的是_____________________________。
a.控制溶液中Fe2+与Fe3+含量比 b.确定下一步还原所需铁的量
c.确定氧化Fe2+所需NaClO3的量 d.确保铁的氧化物酸溶完全
(3)聚合硫酸铁溶液中![]() 与Fe3+物质的量之比不是3∶2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中
与Fe3+物质的量之比不是3∶2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中![]() 与Fe3+物质的量之比。测定时所需的试剂为__________________,需要测定______________和______________的质量。(填写化合物的化学式)
与Fe3+物质的量之比。测定时所需的试剂为__________________,需要测定______________和______________的质量。(填写化合物的化学式)
a.NaOH b.FeSO
查看答案和解析>>
科目:高中化学 来源: 题型:
聚合硫酸铁(PPS)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铁的氧化物为原料来制取聚合硫酸铁,为控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+必须先还原成Fe2+。实验步骤如下:

(1)用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒外,还有______________。
a.容量瓶 b.烧杯 c.烧瓶
(2)步骤Ⅱ取样分析溶液中的Fe2+、Fe3+的含量,目的是_____________________________。
a.控制溶液中Fe2+与Fe3+含量比 b.确定下一步还原所需铁的量
c.确定氧化Fe2+所需NaClO3的量 d.确保铁的氧化物酸溶完全
(3)聚合硫酸铁溶液中![]() 与Fe3+物质的量之比不是3∶2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中
与Fe3+物质的量之比不是3∶2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中![]() 与Fe3+物质的量之比。测定时所需的试剂为__________________,需要测定______________和______________的质量。(填写化合物的化学式)
与Fe3+物质的量之比。测定时所需的试剂为__________________,需要测定______________和______________的质量。(填写化合物的化学式)
a.NaOH b.FeSO4 c.BaCl2 d.NaClO3
查看答案和解析>>
科目:高中化学 来源: 题型:
聚合硫酸铁(PPS)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铁的氧化物为原料来制取聚合硫酸铁,为控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+必须先还原成Fe2+,实验步骤如下:
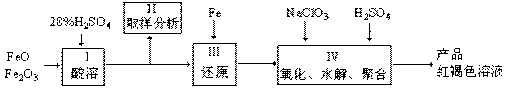
⑴用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒外,还有 。
(a)容量瓶 (b)烧杯 (c)烧瓶
⑵步骤Ⅱ取样分析溶液中的Fe2+、Fe3+的含量,目的是 。
(a)控制溶液中Fe2+与Fe3+含量比 (b)确定下一步还原所需铁的量
(c)确定氧化Fe2+所需NaClO3的量 (d)确保铁的氧化物酸溶完全
⑶用NaClO3氧化时反应方程式如下:6FeSO4+NaClO3+3H2SO4→3Fe2(SO4)3+NaCl+3H2O
若改用硝酸氧化,则反应方程式如下:6FeSO4+2HNO3+3H2SO4→3Fe2(SO4)3+2NO↑+4H2O
已知1mol HNO3价格0.16元、1mol NaClO3价格0.45元,评价用HNO3代替NaClO3作氧化剂的利弊。
利是 ,弊是 。
聚合硫酸铁溶液中SO42-与Fe3+物质的量之比不是3∶2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中SO42-与Fe3+物质的量之比。
⑷测定时所需的试剂 。
(a)NaOH (b)FeSO4 (c)BaCl2 (d)NaClO3
⑸需要测定 和 的质量(填写化合物的化学式)。
⑹选出测定过程中所需要的基本操作 (按操作先后顺序列出)。
(a)萃取、分液 (b)过滤、洗涤 (c)蒸发、结晶(d)冷却、称量 (e)烘干或灼烧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com