
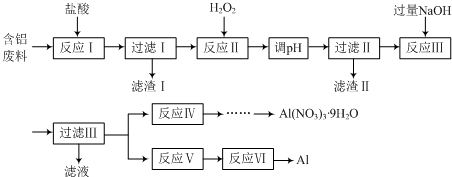
分析 由实验流程可知,加盐酸,Al、Al2O3均转化为Al3+,Fe3O4转化为Fe2+、Fe3+,只有SiO2不反应,则过滤得到的滤渣I为SiO2,反应Ⅱ中过氧化氢与亚铁离子发生氧化还原反应,调节pH使铁离子转化为沉淀,过滤得到的滤渣Ⅱ为Fe(OH)3,反应Ⅲ中铝离子转化为AlO2-,应利用氨水使铝离子转化为Al(OH)3,反应Ⅵ中电解熔融氧化铝得到Al,以此来解答.
解答 解:由实验流程可知,加盐酸,Al、Al2O3均转化为Al3+,Fe3O4转化为Fe2+、Fe3+,只有SiO2不反应,则过滤得到的滤渣I为SiO2,反应Ⅱ中过氧化氢与亚铁离子发生氧化还原反应,调节pH使铁离子转化为沉淀,过滤得到的滤渣Ⅱ为Fe(OH)3,反应Ⅲ中铝离子转化为AlO2-,应利用氨水使铝离子转化为Al(OH)3,反应Ⅵ中电解熔融氧化铝得到Al,
(1)反应Ⅰ中Fe3O4参加反应的离子方程式为Fe3O4+8H+=Fe2++2Fe3++4H2O,故答案为:Fe3O4+8H+=Fe2++2Fe3++4H2O;
(2)反应Ⅱ的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O,故答案为:H2O2+2Fe2++2H+=2Fe3++2H2O;
(3)该流程中有一处设计不合理,指出并加以改正为反应Ⅲ使用过量NaOH错误,应改为氨水,故答案为:反应Ⅲ使用过量NaOH错误,应改为氨水;
(4)反应Ⅵ的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑,故答案为:2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑.
点评 本题考查混合物分离提纯的综合应用,为高频考点,把握流程中的反应、混合物分离方法等为解答的关键,侧重分析与实验能力的考查,注意Fe、Al及其化合物的性质,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 816O、817O、818O互为同素异形体 | |
| B. | 正戊烷、异戊烷、新戊烷互为同系物 | |
| C. | O2与O3互为同位素 | |
| D. | CH3-CH2-OH与CH3-O-CH3互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
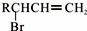 .
.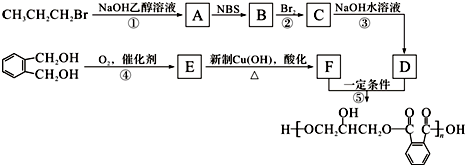
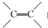 ,C的名称是1,2,3-三溴丙烷.
,C的名称是1,2,3-三溴丙烷.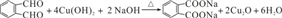 ;
;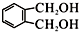 的同分异构体中同时符合下列条件的芳香族化合物共有6种.
的同分异构体中同时符合下列条件的芳香族化合物共有6种.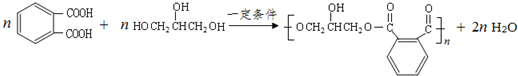 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 mol HI(g) | B. | 2 mol H2(g)和1 mol I2(g) | ||
| C. | 1 mol H2(g)和2 mol I2(g) | D. | 1 mol I2(g)和2 mol HI(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
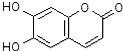
| A. | M的相对分子质量是172 | |
| B. | 1mol M最多能与3mol Br2发生反应 | |
| C. | M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4 | |
| D. | 1mol M与足量Na反应能生成1mol H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
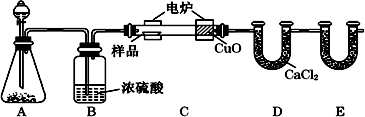
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
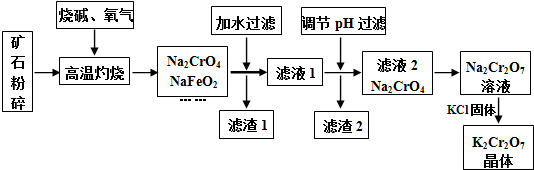
| 时间/(s) | 0 | 0.01 | 0.02 | 0.03 | 0.04 |
| (CrO42-)/(mol•L-1) | 0.20 | 1.6×10-2 | 1.2×10-2 | 1.0×10-2 | |
| (Cr2O72-)/(mol•L-1) | 0 | 9.2×10-2 | 9.4×10-2 | 9.5×10-2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com