
����Ŀ���绯ѧ���ճ���������;�㷺����ͼ����þ����������ȼ�ϵ�ص�ʾ��ͼ������ܷ�ӦʽΪ��Mg+ClO-+H2O�TCl-+Mg(OH)2����ͼ���ǵ�ⷨ��ȥ��ҵ��ˮ�е�Cr2O72-������˵����ȷ����
A. ͼ����Cr2O72-���������缫�ƶ�����ü�������OH-���ת����Cr��OH��3��ȥ
B. ͼ���������ϵĵ缫��ӦʽΪ��Fe-3e-�TFe3+
C. ͼ���з�����������Ӧ�ǣ�ClO-+H2O+2e-�TCl-+2��OH��-
D. ��ͼ����7.2gþ�ܽ�����ĵ�������ͼ�ڷ�ˮ���������ۿɳ�ȥCr2O72-�����ʵ���Ϊ0.05mol
���𰸡�D
��������A��ͼ���ж��Ե缫Ϊ������Fe�缫Ϊ��������Cr2O72-������������缫�ƶ������������ӷ���������ԭ��Ӧ���ɵĽ�������������Ե缫������OH-���ת����Cr��OH��3��ȥ��A����B��ͼ���������ϵĵ缫��ӦʽΪ��Fe-2e-��Fe2+��B����C����ԭ����У�þ��������������þʧ���ӷ���������Ӧ��C����D��n��Mg��=7.2g��24g/mol=0.3mol���ɵ����غ��֪6Mg��6Fe2+��Cr2O72-��������ۿɳ�ȥCr2O72-�����ʵ���Ϊ0.3mol��6��0.05mol��D��ȷ����ѡD��


 ������ҵ��ٳɳ����½������������ϵ�д�
������ҵ��ٳɳ����½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����п�ͼ�е����ʾ�Ϊ���л�ѧ���������ʣ�����A�ǽ������ϵ���Ҫ�ɷ֣�B�����������ͼ������֮����ת����ϵ����ش�

��1��д������A�Ļ�ѧʽ��_____________ ��
��2���õ�F��Һ�IJ�����������Ϊ��________________��
��3����I�Ǻ��ɫ��������д������ת���Ļ�ѧ����ʽ��
B��G��_________________��G + F �� I��__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���᳦��ҩ����Ч�ɷֵĺϳ�·������(���ַ�Ӧ��ȥ�Լ�������):

��֪:(a) 
(b) ![]() (�����ױ�����)
(�����ױ�����)
��ش���������:
��1��D�Ľṹ��ʽΪ____����A�ķ���ʽΪ________��
��2����Ӧ���ķ�Ӧ������__________��
��3�������жԸÿ��᳦��ҩ����Ч�ɷֿ��ܾ��е������Ʋ���ȷ����_______��
A.ˮ���Աȱ��Ӻ� B.�ܷ�����ȥ��Ӧ��Ҳ�ܷ����ۺϷ�Ӧ
C.�����������м��� D.1mol������������4molH2������Ӧ
��E������NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ_______________��
��4���������������Ŀ��᳦��ҩ����Ч�ɷֵ�ͬ���칹����____�֡�
A.��FeCl3��Һ������ɫ��Ӧ
B.�����м��뱽��ֱ������
C.�����Ϲ�������ȡ����
��5����֪���������������ʱ������һ��ȡ��������ȡ����������ڶ�λ�����������������Ȼ�ʱ��ȡ���ڼ�λ���ݴ˰��Ⱥ�˳��д����AΪԭ�Ϻϳ��ڰ��������� (![]() )�ϳ�·���������м����Ľṹ��ʽ(���ַ�Ӧ��������ȥ)��A��________��_________��
)�ϳ�·���������м����Ľṹ��ʽ(���ַ�Ӧ��������ȥ)��A��________��_________��![]() ____________
____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ʵ�Ľ�����ȷ����
ѡ�� | �������ʵ | ���� |
A | ����NaAlO2��Һ���Ի�ù���NaAlO2 | NaAlO2��ˮ�в���ˮ�� |
B | ʩ��ʱ����ľ��(��Ч�ɷ�ΪK2CO3)������NH4Cl���ʹ�� | K2CO3��NH4Cl��Ӧ���ɰ����ή�ͷ�Ч |
C | Ư���ڿ����о��ñ��� | Ư���е�ClO-����ˮ���HClO |
D | FeCl3��Һ������ˮ���� | FeCl3��Fe3+���������Կ�ɱ������ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����Ũ�Ⱦ�Ϊ0.1mol/L������ֱ�ΪVa��Vb��HA��Һ��BOH��Һ����ͬ����Ȼ�ϣ�����Va+Vb=100mL��Va��Vb����ҺpH�Ĺ�ϵ��ͼ��ʾ������˵����ȷ������ ��

A. Ka(HA)=1��10-6mol/L
B. b��c (B+)=c(A-)=c(OH-)=c(H+)
C. c��ʱ��![]() ���¶����߶���С
���¶����߶���С
D. a��c������ˮ�ĵ���̶�ʼ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1L1molL��1NaOH��Һ����0.6molCO2 �� ������Һ��Na2CO3��NaHCO3�����ʵ���֮��ԼΪ�� ��
A.2��3
B.1��2
C.2��1
D.3��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ֲ��Ҷ����ȡ�ľ��ͳɷִ�������ת����ϵ��
![]()
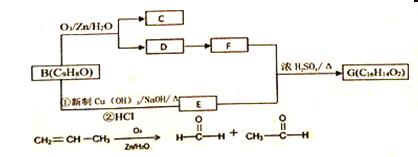
��1��������Dת��ΪFʱ�ķ�Ӧ������__________��A�к��еĹ���������______��
��2�����ڼ�˵����ȷ����________
A.��������Ʒ�Ӧ�ų����� B.1mol���������1molH2�����ӳɷ�Ӧ
C.����һ�����������γɸ߷��ӻ�����
��3��B�����������______��̼ԭ�ӹ���
��4��д��Bת��ΪE�Ļ�ѧ��Ӧ����ʽ��_________________________����____________________________________��
��5��д��E+F��G�Ļ�ѧ��Ӧ����ʽ_________________________��
��6��д����������Ҫ���E��ͬ���칹��Ľṹ��ʽ_____________��
��������ֻ������ȡ���� ����ʹ���CCl4��Һ��ɫ�����������������ܷ���ˮ��
�ۺ˴Ź���������ʾ���շ����֮��1:1:2:2:2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й���ɫ��Ӧ��˵��������ǣ� ��
A.�۲�K2SO4����ɫӦ����ɫ���ܲ���
B.Na��NaCl������ʱ������ɫ��ͬ
C.��������ɫ��Ӧ������NaCl��KCl
D.��ɫ��Ӧһ��������ѧ�仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(V)���仯�������Ź㷺����;����ش���������:
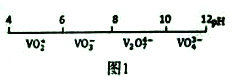
��1��������Һ�е���Ҫ�ۺ�״̬����Һ��pH��ϵ��ͼ1��ʾ��V2O74-��VԪ�صĻ��ϼ���_____����д����Һ��VO3-ת��ΪV2O74-�����ӷ���ʽ:____________��
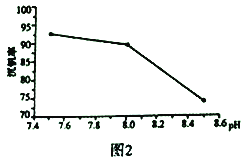
��2�����������γ�������ԭ�����ں��з�Ԫ�ص���Һ�м�����κ��γ�NH4VO3������ͼ2���ڹ�ҵ�����в�ͬpH�����³����ʵIJⶨֵ��ʵ�ʹ�ҵ�����г�ѡ��pH=7.5Ϊ�����������������pH����8.0ʱ�����ʽ��ͣ���ԭ������Һ��VO3-ת��ΪV2O74-��_______��(����д��һ��ԭ��)
��3��NH4VO3�ڸ����·ֽ������V2O5����Ϊ���Ṥҵ��2SO2(g)+O2(g)![]() 2SO3(g) ��H=p�Ĵ��������ԭ����ͼ3��ʾ��
2SO3(g) ��H=p�Ĵ��������ԭ����ͼ3��ʾ��
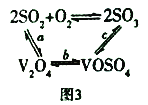
������a����b�Ļ�ѧ����ʽΪ:V2O5(s)+SO2(g)=V2O4(s)+SO3(g)��H=q��
V2O4(s)+O2(g)+2SO2(g)=2VOSO4(g)��H=r
��д������c���Ȼ�ѧ����ʽ:_________________��
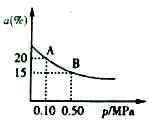
��t2���£���Ӧ:2SO3(g)![]() 2SO2(g)+O2(g)��H>0��SO3��ƽ��ת����(a)����ϵ��ѹǿ(p)�Ĺ�ϵ��ͼ��ʾ��t���£���2molSO3����10L�ܱ������У���Ӧ��ƽ�����ϵ��ѹǿΪ0.10MPa��B��Ļ�ѧƽ�ⳣ����ֵ��__________��
2SO2(g)+O2(g)��H>0��SO3��ƽ��ת����(a)����ϵ��ѹǿ(p)�Ĺ�ϵ��ͼ��ʾ��t���£���2molSO3����10L�ܱ������У���Ӧ��ƽ�����ϵ��ѹǿΪ0.10MPa��B��Ļ�ѧƽ�ⳣ����ֵ��__________��
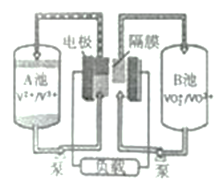
(4)ȫ��ҹ�������һ�ֿɳ���أ�װ����ͼ��ʾ�����ڷŵ��������H+��A������B�أ���:
���ŵ�����У������õ���_______��(����A������B��)��
���������У���������ʽΪ____________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com