
【题目】A、B、C、D、E、W为六种前四周期元素,它们的原子序数依次增大。A与D同主族,可形成DA型离子化合物,B与C同周期且相邻,C与E同主族,E2-与Ar原子具有相同的电子层结构,W的合金用量最大、用途最广。请回答下列问题:
(1)W元素在元素周期表中的位置为 。
(2)下列说法正确的是( )
A.原子半径:A<B<C<D<E
B.D2WC4可以用来做消毒剂和净水剂
C.A4B2C3中既含有离子键又含有共价键
D.D2C2与EC2可以反应生成D2EC3和C2
(3)灼热的碳能与B的最高价氧化物对应水化物的浓溶液反应,化学反应方程式为 。
(4)向盛有A2C2溶液的试管中加入几滴酸化的WEC4溶液,溶液变成棕黄色,发生反应的离子方程式为 ;一段时间后,溶液中有大量气泡出现,随后溶液温度升高,有红褐色沉淀生成,则产生气泡的原因是 ;生成沉淀的原因是 (用平衡移动原理解释)。
【答案】(1)第四周期 Ⅷ族;(2)BC;
(3)C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O;
(4)H2O2+2H++2FE2+=2FE3++2H2O,FE3+催化H2O2分解产生O2,温度升高,促进FE3+水解平衡向正向移动。
【解析】试题分析:A和D属于同主族,可形成DA型离子化合物,此化合物是NaH,即A为H,D为Na,E2-与Ar原子具有相同的电子层结构,即E为S,C与E同主族,即C为O,B与C同周期且相邻,即B为N,W的合金用量最大,与用途最广,即W为FE,(1)铁26号元素,位于第四周期第Ⅷ族;(2)A、半径大小比较:一看电子层数,电子层数越多,半径越大,二看原子序数,电子层数相同,半径随着原子序数的增大而减小,即Na>S>N>O>H,故错误;B、此化合物是Na2FEO4,FEO42-具有强氧化性,能消毒,FE元素被还原成FE3+,FE3+水解成氢氧化铁胶体,能吸附水中悬浮杂质,达到净水的目的,故正确;C、化学式为H4N2O3,为NH4NO3,属于离子化合物,含有离子键,N和H之间、N和O之间含有共价键,故正确;D、D2C2为Na2O2、EC2为SO2,过氧化钠具有强氧化性,发生Na2O2+SO2=Na2SO4,故错误;(3)C和浓硝酸发生反应:C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;(4)A2C2为H2O2,WEC4为FESO4,过氧化氢具有强氧化性,能把FE2+氧化成FE3+,且FE3+作催化剂,使H2O2分解,反应是:H2O2+2H++2FE2+=2FE3++2H2O,FE3+催化H2O2分解产生O2,FE3++3H2O
CO2↑+4NO2↑+2H2O;(4)A2C2为H2O2,WEC4为FESO4,过氧化氢具有强氧化性,能把FE2+氧化成FE3+,且FE3+作催化剂,使H2O2分解,反应是:H2O2+2H++2FE2+=2FE3++2H2O,FE3+催化H2O2分解产生O2,FE3++3H2O![]() FE(OH)3+3H+,水解反应是吸热反应,升高温度使平衡向正反应方向移动,生成红褐色沉淀氢氧化铁。
FE(OH)3+3H+,水解反应是吸热反应,升高温度使平衡向正反应方向移动,生成红褐色沉淀氢氧化铁。


科目:高中化学 来源: 题型:
【题目】下列实验事实可用来证明氨水是弱碱的是
A. 氨水能跟氯化铝溶液反应生成氢氧化铝沉淀
B. 铵盐受热易分解
C. 1mol/L 的氨水可以使酚酞试液变红
D. 常温下0.1mol/L的氯化铵溶液的pH为5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质,工业上通过下述流程回收Na2Cr2O7等物质。
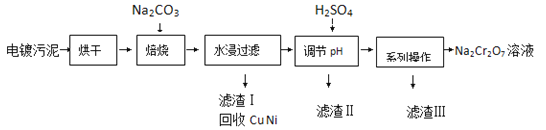
已知:
①Cr(OH)3、ZnO和Al2O3一样均为两性化合物;
②Na2Cr2O7、Na2SO4在不同温度下的溶解度如下表:
20℃ | 60℃ | 100℃ | |
Na2SO4 | 19.5 | 45.3 | 42.5 |
Na2Cr2O7 | 183 | 269 | 415 |
(1)焙烧过程中生成Na2CrO4的化学方程式为 ;水浸后溶液中除Na2CrO4还存在的溶质有 和 ;
(2)加入H2SO4调节pH的目的为 ;
(3)得到滤渣Ⅲ的“系列操作”的步骤为 、 过滤;
(4)若1L加入H2SO4后所得溶液中含铬元素质量为23.4g,CrO42﹣有8/9转化为Cr2O72﹣,求转化后所得溶液中c(Cr2O72﹣) = molL﹣1;
(5)向Na2Cr2O7与H2SO4混合液中加入H2O2,再加入乙醚并摇动,乙醚层为蓝色。乙醚中溶有CrO5,则发生反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组探究FeSO4的化学性质和用途。回答下列问题:
(1)探究FeSO4溶液的酸碱性:取少量FeSO4固体,利用石蕊试液测试FeSO4溶液的酸碱性,必须选用的仪器有胶头滴管、药匙和 。
A.玻璃棒 B.试管 C.天平 D.量筒
(2)利用下图装置探究FeSO4的稳定性
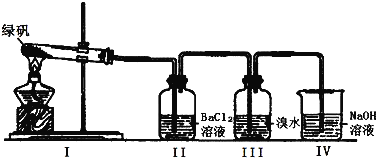
①II中有白色沉淀生成,小组成员结合理论分析,认为下列分解产物不可能的是 。
A.Fe2O3 、SO3 、H2O
B.Fe2O3 、SO2 、SO3 、H2O
C.FeO 、Fe2O3 、SO2 、SO3 、H2O
②III中溴水是用来检验是否有SO2气体生成,若有SO2生成,溴水将褪色。实验中,观察到溴水褪色,据此推测FeSO4分解最有可能被氧化的元素是 。
③NaOH的作用是吸收SO2气体,请写出最大量吸收SO2气体的反应化学方程式: 。
(3)探究FeSO4中Fe2+还原性:
证明FeSO4有较强的还原性,完成下表。
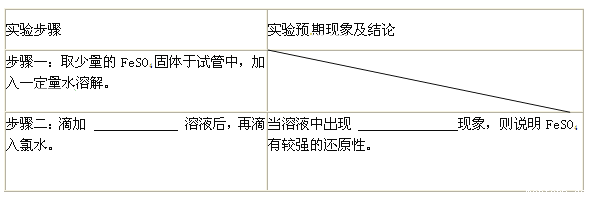
(4)硫酸亚铁用途探究
缺铁性贫血往往口服硫酸亚铁,当用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,其作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 设NA为阿伏伽德罗常数值。下列有关叙述不正确的是
A.将1molCl2溶入足量的水中,溶液里HClO、Cl-、ClO-粒子数之和为2NA
B.3.4g NH3中共用电子对数为0.6NA
C.相同质量的N2和CO所含有的分子数、原子总数、电子总数都相等
D.标准状况下,11.2L由CH4和C2H4组成的混合气体中含有氢原子的数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示
[已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6 kJ·mol-1]:
2SO3(g) ΔH=-196.6 kJ·mol-1]:
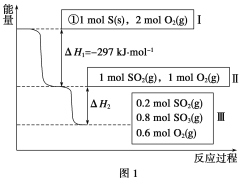
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:____________________。
(2)ΔH2=_____________________。
(3)恒温恒容时,1 mol SO2和2 mol O2充分反应,放出热量的数值比|ΔH2|________(填“大”、“小”或“相等”)。
(4)将Ⅲ中的混合气体通入足量的NaOH溶液中消耗NaOH的物质的量为__________,若溶液中发生了氧化还原反应,则该过程的离子方程式为______________________。
(5)向同温、同体积的三个密闭容器中分别充入气体:(甲)2 mol SO2 和1 mol O2;(乙) 1 mol SO2 和0.5 mol O2;(丙) 2 mol SO3;恒温、恒容下反应达平衡时,下列关系一定正确的是( )
A.容器内压强p:p甲=p丙>2p乙
B.SO3的质量m:m甲=m丙>2m乙
C.c(SO2)与c(O2)之比k:k甲=k丙>k乙
D.反应放出或吸收热量的数值Q:Q甲=Q丙>2Q乙
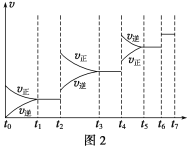
(6)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是__________;图中表示平衡混合物中SO3的含量最高的一段时间是____________。
(7)各阶段平衡时对应的平衡常数如下表所示:
t1~t2 | t3~t4 | t5~t6 | t6~t7 |
K1 | K2 | K3 | K4 |
K1、K2、K3、K4之间的关系为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com