
| 3 |
| 2 |
| 3 |
| 2 |


科目:高中化学 来源: 题型:
| A、减小NH3的浓度 |
| B、增大N2的浓度 |
| C、减小压强 |
| D、降低温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
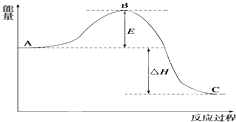 2SO2(g)+O2(g)═2SO3(g),反应过程的能量变化如图所示.已知:1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ/mol.
2SO2(g)+O2(g)═2SO3(g),反应过程的能量变化如图所示.已知:1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ/mol.查看答案和解析>>
科目:高中化学 来源: 题型:
 铜合金是人类使用最早的金属材料,铜在化合物中常见的化合价有+1、+2价,能形成多种铜的化合物.
铜合金是人类使用最早的金属材料,铜在化合物中常见的化合价有+1、+2价,能形成多种铜的化合物.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 反应物 | 反应条件 | 反应类型 | 反应现象及生成物的性质 | |
| A | 苯、液溴 | FeBr3、加热 | 取代反应 | 剧烈沸腾,产生的气体在水面上形成白雾 |
| B | 乙醇、空气 | Cu、加热 | 氧化反应 | Cu在空气中加热变黑,伸入乙醇中变红.重复几次后,乙醇的香味消失,生成有刺激性气味的物质 |
| C | 乙酸、乙醇 | 浓硫酸、 加热 |
酯化反应 | 有不溶于水、比水重且有苦杏仁味的油状液体生成 |
| D | 1mL 20%的蔗糖溶液 | 稀硫酸、 水浴加热 |
取代反应 | 取少量反应后的溶液,加入少量的新制的Cu(OH)2,加热煮沸,产生砖红色沉淀 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2-═Ag2S↓+2Cl- |
| B、Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物:2Na2O2+2CO2═2Na2CO3+O2 |
| C、向酸性KMnO4溶液中加入H2O2:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O |
| D、在0.1mol/L CH3COONa溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com