
| A. | 原子半径 Na<Mg<Al | B. | 酸性 H2SiO3<H2CO3<H2SO4 | ||
| C. | 稳定性 HF<HCl<HBr | D. | 碱性 NaOH<Mg(OH)2<Al(OH)3 |
分析 A.同周期从左向右原子半径减小;
B.非金属性越强,最高价氧化物的水化物酸性越强;
C.非金属性越强,气态氢化物越稳定;
D.金属性越强,最高价氧化物的水化物碱性越强.
解答 解:A.同周期从左向右原子半径减小,则原子半径为Na>Mg>Al,故A错误;
B.非金属性为S>C>Si,最高价氧化物的水化物酸性为H2SiO3<H2CO3<H2SO4,故B正确;
C.非金属性为F>Cl>Br,气态氢化物稳定性为HF>HCl>HBr,故C错误;
D.金属性为Na>Mg>Al,最高价氧化物的水化物碱性为NaOH>Mg(OH)2>Al(OH)3,故D错误;
故选B.
点评 本题考查元素周期表和元素周期律,为高频考点,把握元素的位置、元素性质比较为解答的关键,侧重金属性、非金属性比较的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | C的氧化物是碱性氧化物 | |
| B. | D与A能形成原子个数比为1:1型的离子化合物 | |
| C. | 最高价氧化物对应水化物的酸性:B>A | |
| D. | 工业上电解由A,C两种元素组成的化合物制备C单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向盛有少量Mg(OH)2沉淀的试管中滴加适量NH4Cl溶液,沉淀溶解:Mg(OH)2+2NH4+=2NH3•H2O+Mg2+ | |
| B. | SO2通入澄清石灰水中,产生白色沉淀:SO2+Ca2++2OH-=CaSO4↓+H2O | |
| C. | 向Ca(HCO3)2溶液中加入过量NaOH溶液,有白色沉淀生成:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| D. | 长期过量服用阿司匹林出现水杨酸(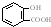 )反应,可静脉注滴NaHCO3溶液: )反应,可静脉注滴NaHCO3溶液: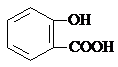 +HCO3-→ +HCO3-→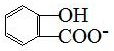 +CO2↑+H2O +CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
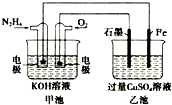
| A. | 甲池中负极上的电极反应式为N2H4-4e-=N2+4H+ | |
| B. | 乙池中石墨电极上发生的反应为4OH--4e-=2H2O+O2↑ | |
| C. | 甲池溶液pH增大,乙池溶液pH减小 | |
| D. | 甲池中每消耗0.1mol N2H4乙池电极上则会析出6.4g固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2可用作漂白剂,原因是具有还原性 | |
| B. | FeCl3溶液可用于制印刷电路板,原因是能氧化Cu | |
| C. | Cl2可制漂白粉,原因是能与NaOH反应 | |
| D. | Al(OH)3可用于治疗胃酸过多,原因是碱性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ④ | ⑤ | ⑥ | ⑨ | ||||
| 3 | ① | ② | ③ | ⑦ | ⑧ |
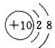 .
.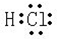 ,
,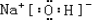 ,所含有的化学键类型有离子键、极性共价键,(请选择“离子键”、“极性共价键”、“非极性共价键”中的一个或几个填写).
,所含有的化学键类型有离子键、极性共价键,(请选择“离子键”、“极性共价键”、“非极性共价键”中的一个或几个填写).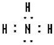 ,其水溶液的pH>7(填“<”或“>”).
,其水溶液的pH>7(填“<”或“>”).查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | H2、I2和HI都是共价化合物 | |
| B. | 断开2 mol HI分子中的化学键所需能量约为(c+b+2a) kJ | |
| C. | 相同条件下,1 mol H2(g)和1mol I2(g)总能量小于2 mol HI (g)的总能量 | |
| D. | 向密闭容器中加入1 mol H2(g)和1 mol I2(g),充分反应后放出的热量为2a kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 苯在常温下可与溴水发生取代反应 | |
| B. | 糖类、油脂和蛋白质都能发生水解反应 | |
| C. | 乙醇和乙酸都能与金属钠反应 | |
| D. | 葡萄糖能发生氧化反应和银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 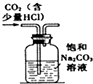 图装置:除去二氧化碳中的少量氯化氢气体 | |
| B. | 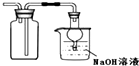 图装置:收集二氧化硫并吸收尾气 | |
| C. |  图装置:用酸性高锰酸钾溶液滴定过氧化氢溶液 | |
| D. |  图装置:用水吸收氯化氢气体并防止倒吸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com