
| 元素 | 甲 | 乙 | 丙 |
| 原子序数 | 6 | 8 | 13 |
| 元素符号 | |||
| 周期 | |||
| 族 |
 ,位于第二周期第ⅣA族;
,位于第二周期第ⅣA族; ,位于第二周期第ⅥA族,
,位于第二周期第ⅥA族, ,位于第三周期第ⅢA族,
,位于第三周期第ⅢA族,| 元素 | 甲 | 乙 | 丙 |
| 原子序数 | 6 | 8 | 13 |
| 元素符号 | C | O | Al |
| 周期 | 二 | 二 | 三 |
| 族 | ⅣA | ⅥA | ⅢA |
| ||
| ||
| ||
| ||


科目:高中化学 来源: 题型:
| A、将试管置于40℃水中,试管中无明显变化 |
| B、将试管置于5℃水中,试管中气泡明显增多 |
| C、向试管中加入少量MnO2,试管中气泡明显增多 |
| D、向试管中加入少量1mol/LFeCl3溶液,试管中无明显变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
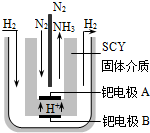 现在普遍应用的工业合成氨的方法是哈伯于1905年发明的,但此法反应物的转化率不高.
现在普遍应用的工业合成氨的方法是哈伯于1905年发明的,但此法反应物的转化率不高.查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 |
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | C | O | F | |||||
| 3 | Na | Mg | P | S | Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| 900~1200℃ |

查看答案和解析>>
科目:高中化学 来源: 题型:
 2012年3月,新《环境空气质量标准》的颁布表明国家对环境问题的进一步重视.
2012年3月,新《环境空气质量标准》的颁布表明国家对环境问题的进一步重视.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com